摘要:25]. 图1中B为电源.电动势ε=27V.内阻不计.固定电阻R1=500Ω.R2为光敏电阻.C为平行板电容器.虚线到两极板距离相等.极板长l1=8.0×10-2m.两极板的间距d=1.0×10-2m.S为屏.与极板垂直.到极板的距离l2=0.16m.P为一圆盘.由形状相同.透光率不同的三个扇形a.b和c构成.它可绕轴转动.当细光束通过扇形a.b.c照射光敏电阻R2时.R2的阻值分别为1000Ω.2000Ω.4500Ω.有一细电子束沿图中虚线以速度v0=8.0×105m/s连续不断地射入C.已知电子电量ε=1.6×10-13C.电子质量m=9×10-31kg.忽略细光束的宽度.电容器的充电放电时间及电子所受的重力.假设照在R2上的光强发生变化时R2阻值立即有相应的改变. (1)设圆盘不转动.细光束通过b照射到R2上.求电子到达屏S上时.它离O点的距离y.(计算结果保留二位有效数字). (2)设转盘按图1中箭头方向匀速转动.每3秒转一圈.取光束照在a.b分界处时t=0.试在图2给出的坐标纸上.画出电子到达屏S上时.它离O点的距离y随时间的变化图线. 要求在y轴上标出图线最高点与最低点的值.(不要求写出计算过程.只按画出的图线评分.) [26].已知A.B.C.D为气体.E.F为固体.G是氯化钙.它们之间的转换关系如下图所示: 是 .E的化学式是 . (2)A和B反应生成C的化学方程式是 . (3)E和F反应生成D.H和G的化学方程式是 .
网址:http://m.1010jiajiao.com/timu3_id_35749[举报]
在实验室里可用如图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.
图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.请填写下列空白:
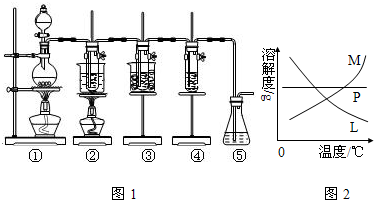
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:①
(4)反应完毕经冷却后,②的试管中有大量晶体析出.如图2中符合该晶体溶解度曲线的是
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1:2,则该反应中氧化剂和还原剂的物质的量之比为:
查看习题详情和答案>>
图1中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.请填写下列空白:

(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A、C
A、C
.(已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3)A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:①
制取温度不同
制取温度不同
; ②制取时碱的浓度也不同
制取时碱的浓度也不同
.(4)反应完毕经冷却后,②的试管中有大量晶体析出.如图2中符合该晶体溶解度曲线的是
M
M
(填写编号字母);从②的试管中分离出该晶体的方法是过滤
过滤
(填写实验操作名称).(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性
不可
不可
.为什么?石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
.(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1:2,则该反应中氧化剂和还原剂的物质的量之比为:
7:3
7:3
.(2008?镇江二模)下列图1中B是一种常见的无色无味的液体.C是一种有磁性的化合物,E是一种无色无味的有毒气体.根据下列图1、图2,回答下列问题:

(1)写出C的化学式:
(2)E和N2是等电子体,请写出可能E的电子式:
 .
.
(3)在101kPa和150℃时,可逆反应E(g)+B(g) F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16g G和足量的A反应放出的热量为Q kJ(Q>0),写出这个反应的热化学方程式:
若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式:
查看习题详情和答案>>

(1)写出C的化学式:
Fe3O4
Fe3O4
.(2)E和N2是等电子体,请写出可能E的电子式:


(3)在101kPa和150℃时,可逆反应E(g)+B(g)
 F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)B、C
B、C
. A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16g G和足量的A反应放出的热量为Q kJ(Q>0),写出这个反应的热化学方程式:
S(s)+Fe(s) =FeS(s);△H=-2Q kJ?mol-1
S(s)+Fe(s) =FeS(s);△H=-2Q kJ?mol-1
.若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式:
C6H5OH
C6H5OH
;H的水溶液呈酸性,请用离子方程式表示呈酸性的原因:Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
 Fe(OH)3+3H+
Fe(OH)3+3H+Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
. Fe(OH)3+3H+
Fe(OH)3+3H+在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.

图1中:①为氯气发生装置;
②的试管里盛有15mL 30% KOH溶液,并置于水浴中;
③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.请填写下列空白:
(1)写出装置③发生的化学反应方程式
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
(4)反应完毕经冷却后,②的试管中有大量晶体析出.图2、3中符合该晶体溶解度曲线的是
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1:2,则该反应中氧化剂和还原剂的物质的量之比为:
查看习题详情和答案>>

图1中:①为氯气发生装置;
②的试管里盛有15mL 30% KOH溶液,并置于水浴中;
③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.请填写下列空白:
(1)写出装置③发生的化学反应方程式
2NaOH+Cl2=NaCl+NaClO+H2O
2NaOH+Cl2=NaCl+NaClO+H2O
.(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是:
AC
AC
.(已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3)A.NaBiO3 B.FeCl3 C.PbO2 D.Na2O2
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是①
制取温度不同
制取温度不同
; ②制取时碱的浓度也不同
制取时碱的浓度也不同
.(4)反应完毕经冷却后,②的试管中有大量晶体析出.图2、3中符合该晶体溶解度曲线的是
M
M
(填写编号字母);从②的试管中分离出该晶体的方法是过滤
过滤
(填写实验操作名称).(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性
否
否
.为什么?石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
石蕊溶液褪色的是因为HClO的强氧化性而不是Cl2
.(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1:2,则该反应中氧化剂和还原剂的物质的量之比为:
7:3
7:3
.每年由于腐蚀造成的钢铁损失约占年产量的10~20%,金属的防腐十分重要。钢铁防腐方法有许多种,图—1与图—2是两个典型的例子。对其中原理的描述正确的是 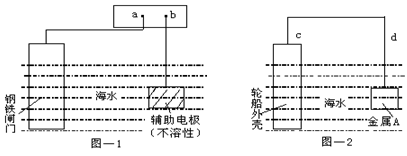
| A.图—1:a为电源正极 | B.图—1:辅助电极上的反应:O2+4e+2H2O→4OH- |
| C.图—2:电子流动方向d→c | D.图—2:金属A可以是耐腐蚀的金属铜 |
下列图1中B是一种常见的无色无味的液体。C是一种有磁性的化合物,E是一种无色无味的有毒气体。根据下列图1、图2,回答下列问题:
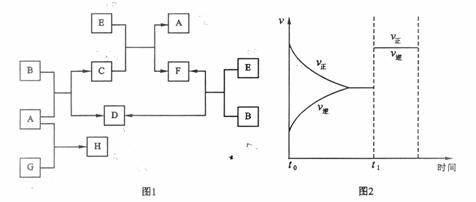
(1)写出C的化学式: 。
(2)E和N2是等电子体,请写出可能E的电子式:
(3)在101kPa和150℃时,可逆反应E(g) + B(g)![]() F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) 。
F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) 。
A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16 g G和足量的A反应放出的热量为Q kJ(Q > 0),写出这个反应的热化学方程式: 。
若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式: ;H的水溶液呈酸性,请用离子方程式表示呈酸性的原因:
查看习题详情和答案>>