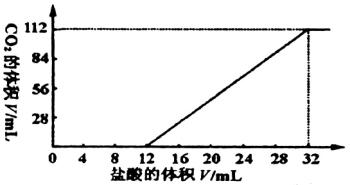
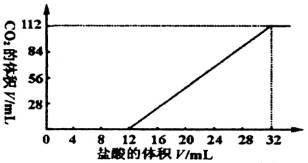
摘要:今有碱金属的两种碳酸盐和碱土金属的一种不溶性碳酸盐组成的混合物.取其7.560g与过量盐酸完全反应.放出CO2体积为1.344L.另取等质量的原混合物.加水搅拌.可滤出不溶性盐1.420g. (1) 取过滤后滤液的1/10体积.向其中缓慢滴加浓度为0.2500mol/L盐酸.并同时记录放出的CO2体积和消耗盐酸的体积.得到如下图所示的曲线. 试计算确定这两种碱金属碳酸盐的化学式. (2) 将过滤出的不溶性盐投入到浓度为2.500mol/L的盐酸中.当完全反应时.耗去盐酸10.O0ml.试计算确定原不溶性碳酸盐的化学式. [答案](1)K2CO3 KHCO3 (2)Mg2(OH)2CO3
网址:http://m.1010jiajiao.com/timu3_id_357337[举报]
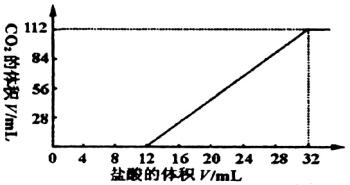
今有碱金属的两种碳酸盐和碱土金属(Mg、Ca等二价金属)的一种不溶性碳酸盐组成的混合物。取7.560 g该混合物与过量盐酸完全反应,放出CO2体积为1.344 L(标准状况)。另取等质量的原混合物加水搅拌,可滤出不溶性盐1.420 g。取过滤后滤液的![]() 体积,向其中缓慢滴加浓度为0.2500 mol/L的盐酸,并同时记录放出的CO2的体积(标准状况)和消耗盐酸的体积,得到如图所示的曲线。通过计算,确定这两种碱金属碳酸盐的化学式。
体积,向其中缓慢滴加浓度为0.2500 mol/L的盐酸,并同时记录放出的CO2的体积(标准状况)和消耗盐酸的体积,得到如图所示的曲线。通过计算,确定这两种碱金属碳酸盐的化学式。
查看习题详情和答案>>