摘要:某种干燥粉末混合物可能由中的两种或几种组成.若将其先与足量盐酸反应则逸出气体a.当a缓慢通过足量的NaOH溶液时气体体积缩小.但仍有剩余.另取原混合物在空气中加热至气体不再发生.发现剩余固体的质量增加.则对原混合物的叙述正确的是 (A)一定含有 (B) 一定含有 和NaCl (C)不含有 (D) 不含有
网址:http://m.1010jiajiao.com/timu3_id_356588[举报]
某种干燥粉末混合物可能由Na2O、Na2CO3、Na2O2、NaCl、NaHCO3中的两种或几种组成(假设固体混合时不反应)。若将其先与足量盐酸反应则逸出气体a,当a缓慢通过足量NaOH溶液时气体体积缩小(同温、同压),但仍有剩余。另取原混合物在空气中加热至气体不再发生,发现剩余固体的质量增加,则对原混合物的叙述正确的是
A.一定含有Na2O、Na2O2、NaHCO3 B.一定含有Na2O和NaCl
C.不含有Na2CO3和Na2O2 D.不含有NaHCO3和Na2CO3
查看习题详情和答案>>某化学兴趣小组有一次活动的内容是:对一包干燥的红色粉末组成进行探究.请你参与并回答有关问题.
教师提醒:它由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成.
提出猜想:红色粉末可能的组成有:
①只有Cu ②只有Fe2O3
③只有Fe(OH)3④是Fe2O3、Fe(OH)3的混合物
⑤是Cu、Fe2O3的混合物 ⑥是Cu、Fe(OH)3的混合物
资料获悉:(1)2Fe(OH)3
Fe2O3+3H2O
(2)白色无水CuSO4遇水变蓝
(3)Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
探究思路:利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成.
(装置内空气中的水蒸气、CO2忽略不计)
实验探究:
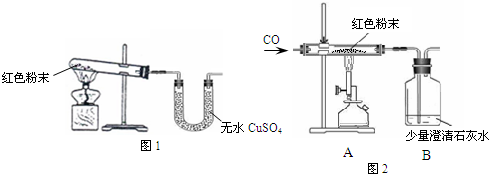
(1)甲同学取适量红色粉末装入试管中,按图1进行实验.结果无水CuSO4没有变蓝,从而排除猜想中的 .(填猜想中的序号)
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色.乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为 的观点正确(填“乙”“丙”).
(3)丁同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按图2在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
交流讨论:
(1)在装置A中先通CO气体的作用是 .
(2)应该选择 组的实验数据计算来确定红色粉末的组成.最终计算结果表明:该红色粉末的组成是猜想中的第 组(填序号).
(3)写出A装置中发生反应的化学方程式 ;实验中观察到A装置中的现象为 .
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处? (填“需要”或“不需要”),理由是 .
反思评价:戊同学指出:从环保角度,图2装置有严重不足之处.你认为应该如何改进? .
拓展延伸:有同学提出丁同学上述实验中的CO还可以用H2代替,并将图28-2中B装置换成盛有碱石灰(生石灰和氢氧化钠固体混合物)的干燥管,来确定该红色粉末的组成,你认为是否可行? (填“可行”或“不可行”).
查看习题详情和答案>>
教师提醒:它由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成.
提出猜想:红色粉末可能的组成有:
①只有Cu ②只有Fe2O3
③只有Fe(OH)3④是Fe2O3、Fe(OH)3的混合物
⑤是Cu、Fe2O3的混合物 ⑥是Cu、Fe(OH)3的混合物
资料获悉:(1)2Fe(OH)3
| ||
(2)白色无水CuSO4遇水变蓝
(3)Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
探究思路:利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成.
(装置内空气中的水蒸气、CO2忽略不计)
实验探究:

(1)甲同学取适量红色粉末装入试管中,按图1进行实验.结果无水CuSO4没有变蓝,从而排除猜想中的
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色.乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为
(3)丁同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按图2在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
| 反应前 | 反应后 | |
| Ⅰ 组 |
玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ 组 |
洗气瓶和所盛溶液 的总质量为180.0g |
洗气瓶和瓶中物质 的总质量为183.1g |
(1)在装置A中先通CO气体的作用是
(2)应该选择
(3)写出A装置中发生反应的化学方程式
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?
反思评价:戊同学指出:从环保角度,图2装置有严重不足之处.你认为应该如何改进?
拓展延伸:有同学提出丁同学上述实验中的CO还可以用H2代替,并将图28-2中B装置换成盛有碱石灰(生石灰和氢氧化钠固体混合物)的干燥管,来确定该红色粉末的组成,你认为是否可行?
某化学兴趣小组有一次活动的内容是:对一包干燥的红色粉末组成进行探究.请你参与并回答有关问题.
教师提醒:它由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成.
提出猜想:红色粉末可能的组成有:
①只有Cu ②只有Fe2O3
③只有Fe(OH)3④是Fe2O3、Fe(OH)3的混合物
⑤是Cu、Fe2O3的混合物 ⑥是Cu、Fe(OH)3的混合物
资料获悉:(1)2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
(2)白色无水CuSO4遇水变蓝
(3)Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
探究思路:利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成.
(装置内空气中的水蒸气、CO2忽略不计)
实验探究:

(1)甲同学取适量红色粉末装入试管中,按图1进行实验.结果无水CuSO4没有变蓝,从而排除猜想中的______.(填猜想中的序号)
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色.乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为______的观点正确(填“乙”“丙”).
(3)丁同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按图2在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ 组 | 洗气瓶和所盛溶液 的总质量为180.0g | 洗气瓶和瓶中物质 的总质量为183.1g |
(1)在装置A中先通CO气体的作用是______.
(2)应该选择______组的实验数据计算来确定红色粉末的组成.最终计算结果表明:该红色粉末的组成是猜想中的第______组(填序号).
(3)写出A装置中发生反应的化学方程式______;实验中观察到A装置中的现象为______.
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?______(填“需要”或“不需要”),理由是______.
反思评价:戊同学指出:从环保角度,图2装置有严重不足之处.你认为应该如何改进?______.
拓展延伸:有同学提出丁同学上述实验中的CO还可以用H2代替,并将图28-2中B装置换成盛有碱石灰(生石灰和氢氧化钠固体混合物)的干燥管,来确定该红色粉末的组成,你认为是否可行?______(填“可行”或“不可行”). 查看习题详情和答案>>
从分类角度看,金属可分为黑色金属和有色金属.铁是日常生活中最常见的黑色金属,请回答下列问题:
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是
A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?
(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为
问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在
(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?
(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是
查看习题详情和答案>>
问题1:铁为何称为黑色金属?
(1)同学们经百度查询,得到以下两种解释,你认为下列解释正确的是
A
A
.(填字母)A.因为铁表面上有黑色的铁的氧化物,所以叫黑色金属.
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属.
(2)已知某黑色粉末为铁和四氧化三铁的混合物.请定性证明其中含有Fe3O4(只要求简述实验方法)?
用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测显蓝色或用纯净的CO与黑色粉末加热反应,用澄清石灰水检验有白色沉淀生成,说明其中含有Fe3O4
用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测显蓝色或用纯净的CO与黑色粉末加热反应,用澄清石灰水检验有白色沉淀生成,说明其中含有Fe3O4
.(3)将适量FeO粉末溶于过量稀硫酸中,并将所得溶液分为两份.一份溶液加入少量硝酸钾晶体,发现溶液颜色发生改变,此反应的离子方程式为
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
,另一份溶液加入一定量氢氧化钠溶液,所见主要实验现象为产生白色絮状沉淀,并迅速变成灰绿色,最后变成红褐色
产生白色絮状沉淀,并迅速变成灰绿色,最后变成红褐色
.问题2:已知CuO在高温时可分解为Cu2O和O2,为探究Fe2O3高温灼烧时是否分解为FeO和O2,同学们设想了两种探究方法:
C.看灼烧前后固体颜色是否变化. D.看灼烧前后固体质量改变情况.
(4)实验时应将Fe2O3放在
坩埚
坩埚
中灼烧.(填仪器名称)(5)方法C中,如果高温灼烧后固体颜色发生明显改变,说明Fe2O3发生了变化.能否说明产物一定为FeO?
不能
不能
,(填“能”或“不能”)理由是Fe3O4也是黑色的
Fe3O4也是黑色的
.(6)方法D中,测得实验结果是固体灼烧前后的质量比为30:29,则高温灼烧后固体生成物是
Fe3O4
Fe3O4
.(2013?安徽模拟)铜陵有色股份有限公司电线电缆厂属国家电线电缆、绕组线行业专业生产厂.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.
甲同学根据已学知识,提出了一套回收方案:

乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O2
2CuSO4+2H2O),于是他提出了另一套方案:

(1)甲方案的①、③两个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:
①
(2)从环保角度对两套方案的不同部分进行比较,你认为
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是:
丁又提出了疑问:“如果铁过量,剩余的铁粉会混在红色粉末中,该怎么处理呢?”.
请提出你的想法:
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.如果直接排放掉滤液,不仅造成了浪费,还会
(5)若上述方案所用的稀硫酸质量分数为36.8%,问每1000mL98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸
查看习题详情和答案>>
甲同学根据已学知识,提出了一套回收方案:

乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O2
| ||

(1)甲方案的①、③两个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:
①
2Cu+O2
2CuO
| ||
2Cu+O2
2CuO
; ③
| ||
Fe+CuSO4═FeSO4+Cu
Fe+CuSO4═FeSO4+Cu
.(2)从环保角度对两套方案的不同部分进行比较,你认为
乙
乙
(填“甲”或“乙”)的方案更合理.理由是:甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾
甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾
.(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是:
将Cu完全置换出来
将Cu完全置换出来
.丁又提出了疑问:“如果铁过量,剩余的铁粉会混在红色粉末中,该怎么处理呢?”.
请提出你的想法:
所得铜粉酸洗后再洗涤、干燥
所得铜粉酸洗后再洗涤、干燥
.(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.如果直接排放掉滤液,不仅造成了浪费,还会
造成水污染或环境污染
造成水污染或环境污染
.(5)若上述方案所用的稀硫酸质量分数为36.8%,问每1000mL98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸
4900
4900
g,需水3060
3060
mL(水的密度为1.0g/mL),在实验室中稀释浓硫酸时,是如何操作的:将浓硫酸沿烧杯内壁缓缓加入水中,边加边搅拌
将浓硫酸沿烧杯内壁缓缓加入水中,边加边搅拌
.