摘要:已知H2PO4-以电离为主.在0.1mol/L的NaH2PO4溶液中,下列微粒浓度关系不正确的是 A.c(Na+)+c(H+)=c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-) B.c(H3PO4)+ c(H+)= c(OH-)+ c(HPO42-)+2c(PO43-) C.c(Na+)=3c(PO43-)+2c(HPO42-)+c(H2PO4-)+ c(H3PO4) D.c(Na+)>c(H2PO4-)>c(H+)>c(HPO42-)>c(H3PO4)
网址:http://m.1010jiajiao.com/timu3_id_356399[举报]
自20世纪90年代以来,芳炔类大环化合物的研究发展十分迅速,具有不同分子结构和几何形状的这一类物质在高科技领域有着十分广泛的应用前景.合成芳炔类大环的一种方法是以苯乙炔(结构简式CH≡C- ,可以简写为
,可以简写为
≡- )为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
)为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
(1)上述系列中第1种物质的分子式为
(2)已知上述系列第1至第4种物质的分子直径在1~100nm之间,分别将它们溶解于有机溶剂中,形成的分散系为
(3)仔细分析以苯乙炔为基本原料,经过一定反应而得到最终产物时苯乙炔组成上的变化.假设反应过程中原料无损失,理论上消耗苯乙炔与所得芳炔类大环化合物的质量比为
(4)已知:以乙醇做溶剂CH2Br-CH2Br(1,2-二溴乙烷)与NaOH加热可以反应生成CH≡CH和NaBr等,该反应化学上称为消去反应.写出其方程式:

在实验中,制备上述系列化合物的原料苯乙炔可用苯乙烯(CH2=CH- )与Br2为主要起始物质,通过加成、消去两步反应制得.写出由苯乙烯制取苯乙炔的两步化学方程式(其他试剂自选).
)与Br2为主要起始物质,通过加成、消去两步反应制得.写出由苯乙烯制取苯乙炔的两步化学方程式(其他试剂自选).


 .
.
查看习题详情和答案>>
 ,可以简写为
,可以简写为≡-
 )为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
)为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
(1)上述系列中第1种物质的分子式为
C24H12
C24H12
(2)已知上述系列第1至第4种物质的分子直径在1~100nm之间,分别将它们溶解于有机溶剂中,形成的分散系为
胶体
胶体
(3)仔细分析以苯乙炔为基本原料,经过一定反应而得到最终产物时苯乙炔组成上的变化.假设反应过程中原料无损失,理论上消耗苯乙炔与所得芳炔类大环化合物的质量比为
51:50
51:50
(4)已知:以乙醇做溶剂CH2Br-CH2Br(1,2-二溴乙烷)与NaOH加热可以反应生成CH≡CH和NaBr等,该反应化学上称为消去反应.写出其方程式:


在实验中,制备上述系列化合物的原料苯乙炔可用苯乙烯(CH2=CH-
 )与Br2为主要起始物质,通过加成、消去两步反应制得.写出由苯乙烯制取苯乙炔的两步化学方程式(其他试剂自选).
)与Br2为主要起始物质,通过加成、消去两步反应制得.写出由苯乙烯制取苯乙炔的两步化学方程式(其他试剂自选).



已知元素的电负性与元素的化合价一样,也是元素的一种基本性质.下面给出14种元素的电负性.
根据以上的数据,可推知元素的电负性具有的变化规律是:
查看习题详情和答案>>
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2. | 1.5 | 2.5 | 2.8 | 4. | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化
在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化
.(2013?武汉模拟)已知: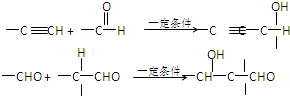
以乙炔为原料,通过如图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产物已略去).

其中,A、B、C、D分别代表一种有机物;B的化学式为C4H10O2,分子中无甲基.
请回答下列问题:
(1)A→B的化学反应类型是
(2)写出生成A的化学方程式:
 .
.
(3)B在浓硫酸催化下加热,可生成多种有机物.写出2种相对分子质量比A小的有机物的结构简式:
(4)写出C生成D的化学方程式:
 .
.
(5)含有苯环,且与E互为同分异构体的酯有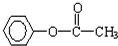 、
、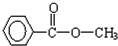 等
等 、
、 等.
等.
查看习题详情和答案>>

以乙炔为原料,通过如图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产物已略去).

其中,A、B、C、D分别代表一种有机物;B的化学式为C4H10O2,分子中无甲基.
请回答下列问题:
(1)A→B的化学反应类型是
加成反应
加成反应
.(2)写出生成A的化学方程式:


(3)B在浓硫酸催化下加热,可生成多种有机物.写出2种相对分子质量比A小的有机物的结构简式:
CH2=CH-CH2CH2OH
CH2=CH-CH2CH2OH
、CH2=CH-CH=CH2
CH2=CH-CH=CH2
.(4)写出C生成D的化学方程式:


(5)含有苯环,且与E互为同分异构体的酯有
5
5
种,写出其中二种同分异构体的结构简式: 、
、 等
等 、
、 等
等(1)将NH3和PH3两分子中的共价键的各种键参数的数值大小相比较的结果是,键长:NH3
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物.PH3分子的空间构型是
(3)二氯化硫(Cl-S-S-Cl)是一种琥珀色液体,是合成硫化染料的重要原料.
①写出它的电子式
 .
.
②指出它分子内的键型
③若4个原子不共面,则该分子
④指出硫元素的化合价为
查看习题详情和答案>>
小于
小于
PH3、键能:NH3大于
大于
PH3(填“大于”、“小于”或“等于”).已知P的电负性小于H,则H为-1
-1
价.(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物.PH3分子的空间构型是
三角锥型
三角锥型
;N2H4分子中氮原子轨道的杂化类型是sp3
sp3
.(3)二氯化硫(Cl-S-S-Cl)是一种琥珀色液体,是合成硫化染料的重要原料.
①写出它的电子式


②指出它分子内的键型
S-S键是非极性共价键,S-Cl是极性共价键
S-S键是非极性共价键,S-Cl是极性共价键
(填“极性”或“非极性”)③若4个原子不共面,则该分子
有
有
(填“有”或“无”)极性.④指出硫元素的化合价为
+1
+1
. 下列说法正确的是( )
下列说法正确的是( )