摘要:一个的原子质量为mg.若阿伏加德罗常数N0.下列式子中可表示一个原子质量的是( ) A. B. C. D.
网址:http://m.1010jiajiao.com/timu3_id_355115[举报]
Wg某元素(无同位素)所含原子数目为n,该元素原子的摩尔质量为Mg/mol,则氯元素的一种同位素35Cl的一个原子的质量是( )(注:该Cl原子的相对原子质量≈35)
A、
| ||
B、
| ||
C、
| ||
D、
|
 下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.| a | b | ||||||||||||||||
| c | d | e | |||||||||||||||
| f | |||||||||||||||||
H2O
H2O
(用化学式填空),其原因是O元素的非金属性大于C元素,且水中存在氢键,导致水的熔点大于甲烷
O元素的非金属性大于C元素,且水中存在氢键,导致水的熔点大于甲烷
.(2)a和d可形成不同晶体,下列说法正确的是(NA是阿佛加德罗常数)
ad
ad
.A.元素a的单质可能是原子晶体或分子晶体
B.mg d元素形成的晶体中,含共价键数目为m NA/7
C.元素a与元素d形成的化合物40g,含NA个分子
D.元素d的最高价氧化物6g,含共价键物质的量为0.4mol
(3)c和e形成的化合物的中,每个阳离子周围距离最近且等距离的阳离子有
12
12
个,一个晶胞中的阴离子数目为4
4
个.晶体中阳离子和阴离子核间距为a cm,该化合物相对分子质量为M,NA为阿伏加德罗常数,则晶体密度为| M |
| 2a3NA |
| M |
| 2a3NA |
(4)f原子的外围电子排布式为
3d64s2
3d64s2
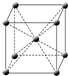
,其晶胞结构如图,f单质的晶体密度为ρg/cm3,f相对原子质量为M,阿伏伽德罗常数NA,则f的原子半径为
| ||
| 4 |
| 3 |
| ||
| ||
| 4 |
| 3 |
| ||
 【化学-选修物质结构与性质】
【化学-选修物质结构与性质】已知A、B、C、D均为周期表中前36号元素,且原子序数依次增大.A、B、C为同一周期的主族元素,A原子最外层有3个未成对电子,B原子p能级电子总数与s能级电子总数相等.D是周期表1-18列中的第10列元素.请回答:
(l)C的电子排布图为
(2)A、B两元素的第一电离能较大的是
(3)A的氢化物的VSEPR模型立体结构为
(4)D属于元素周期表中第
(5)元素D的氧化物DO晶体结构与NaCl晶体结构相同,已知D2+与最近O2-的核间距离为acm,DO的摩尔质量为Mg/mol,若用“NAA表示阿伏加德罗常数,则DO晶体的密度为
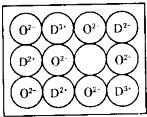
(6)天然的和绝大部分人工制备的晶体都存在各种缺陷,某种DO晶体中就存在如图所示的缺陷:一个D2+空缺,另有两个D2+被两个D3+所取代.其结果晶体仍呈电中性,但化合物中D和O的比值却发生了变化.其氧化D样品组成为D0.97O,则该晶体中D3+与D2+的离子个数比为
下表为元素周期表的一部分。请回答下列问题:
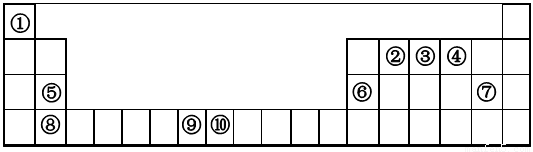
根据元素在周期表中的相对位置可知①~⑩分别是H、C、N、O、Mg、Al、Cl、Ca、Mn、Fe。
(1)上述元素中,属于s区的是____________(填元素符号)。
(2)写出元素④的基态原子的价电子排布图____________________。
(3)元素第一电离能为⑨________⑩ (填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_____________________________。
(5)⑥单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
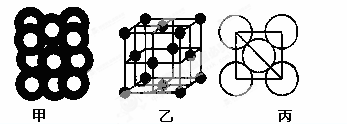
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数,元素⑥的相对原子质量为M,请回答:晶胞中⑥原子的配位数为 ,该晶体的密度为 (用字母表示)
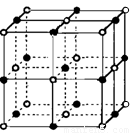
(6)实验证明:⑤和⑧的氧化物、KCl、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表:
|
离子晶体 |
NaCl |
KCl |
CaO |
|
晶格能/kJ·mol-1 |
786 |
715 |
3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是: (用化学式填写)。
其中⑧的氧化物晶体中一个阳离子周围和它最邻近且等距离的阳离子有 个。
查看习题详情和答案>>