摘要:12.铜与氯化铁溶液
网址:http://m.1010jiajiao.com/timu3_id_354266[举报]
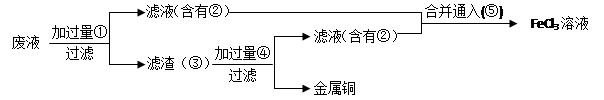
氯化铁能腐蚀铜(2FeCl3+Cu═2FeCl2+CuCl2),工业上常用此原理生产印刷线路板(步骤Ⅰ).从废液中回收铜并使FeCl3溶液循环利用的主要流程如图所示:

(1)写出步骤Ⅱ中发生反应的一个离子方程式 .
(2)向滤液B中加入适量的H2O2可得到FeCl3溶液并循环使用.试写出该反应的化学方程式 .
(3)某校化学小组的同学用如图装置对铜与浓硫酸在一定条件下的反应进行实验探究,请回答:
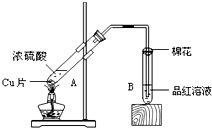
Ⅰ.若A中有1mol Cu完全反应,则被还原的H2SO4的物质的量为 .
Ⅱ.B试管管口堵的棉花可以事先用下列 试剂浸泡(填序号).
①酸性高锰酸钾溶液 ②浓硫酸 ③NaOH溶液. 查看习题详情和答案>>

(1)写出步骤Ⅱ中发生反应的一个离子方程式
(2)向滤液B中加入适量的H2O2可得到FeCl3溶液并循环使用.试写出该反应的化学方程式
(3)某校化学小组的同学用如图装置对铜与浓硫酸在一定条件下的反应进行实验探究,请回答:

Ⅰ.若A中有1mol Cu完全反应,则被还原的H2SO4的物质的量为
Ⅱ.B试管管口堵的棉花可以事先用下列
①酸性高锰酸钾溶液 ②浓硫酸 ③NaOH溶液. 查看习题详情和答案>>
已知氯化铁溶液能与铜反应,生成氯化亚铁和氯化铜。现将Fe、FeCl2溶液、FeCl3溶液、Cu、CuCl2溶液放入同一容器中,充分反应后:
(1)若溶液中有较多量的Fe2+,且有铁剩余,则容器内还可能有5种物质中的____________。
(2)若溶液中有较多量的Cu2+,则容器内还可能有5种物质中的______________________。
(3)若溶液中有较多量的Cu2+,且有铜剩余,则容器内还可能有5种物质中的___________。
(4)若溶液中有较多量的Fe3+和Cu2+,则容器内还可能有5种物质中的__________________。
查看习题详情和答案>>已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式(1分):
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤: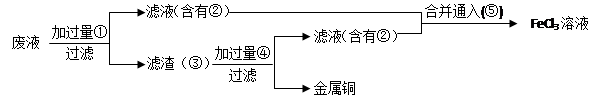
A.请写出上述实验中加入或生成的有关物质的化学式:
① ,② ,④ ,
B.请写出含有②的滤液与⑤反应的离子方程式(1分):
该反应中氧化剂为 还原剂为 。