网址:http://m.1010jiajiao.com/timu3_id_354181[举报]
(10分)(1) 已知某粒子的结构示意图为:
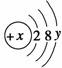 试回答:
试回答:
① 当x-y=10时,该粒子为 (填“原子”、“阳离子”或“阴离子”)。
?② 当y=8时,阳离子或阴离子可能为(填离子符号): 、 、 、 。
若它们形成化合物时离子数之比为1︰2,则这些化合物的电子式为 、 。
(2) 原子序数大于4 的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:
元素A 和B 所属周期序数之差为 ;元素A 和B 的原子序数之差为 ;元素B 和A 的最高化合价之差为 。
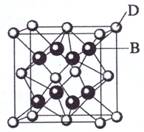
查看习题详情和答案>>(10分)已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如右图。请回答:
(1)A与B形成的化合物在固态时的晶体类型是 ;A与B形成的化合物比A与C形成的化合物熔点要____(填高、低)
(2)写出C的单质与水反应的离子方程式 ;
(3)如图所示,D跟B形成的离子化合物的化学式为 ;鉴别该离子化合物是否为晶体,最可靠的科学方法是 ,该离子化合物晶体的密度为ag·cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是 cm3(只要求列出算式)。
【解析】在前36号元素中,符合周期表中1—18列中的第8列元素的是铁,即E是铁,则D是Ca。根据D跟B形成离子化合物晶胞结构可判断,该离子化合物是DB2,则B是F或Cl。因为B和C属同一主族,且原子序数前者小于后者,所以B只能是F,C是Cl,A与其他4种元素既不在同一周期又不在同一族,所以A是H。
(1)HF属于分子晶体,由于HF中含有氢键,所以HF的沸点高于氯化氢的。
(2)氯气溶于水生成盐酸和次氯酸。
(3)鉴别离子化合物是否为晶体,最可靠的科学方法是射线衍射法。在该晶胞中含有的该离子是8×1/8+6×1/2=4,则F-是8,所以晶胞的体积是(8b+4c)/a NA。
查看习题详情和答案>>
(10分)已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如右图。请回答:
 (1)A与B形成的化合物在固态时的晶体类型是
;A与B形成的化合物比A与C形成的化合物熔点要____(填高、低)
(1)A与B形成的化合物在固态时的晶体类型是
;A与B形成的化合物比A与C形成的化合物熔点要____(填高、低)
(2) 写出C的单质与水反应的离子方程式
;
写出C的单质与水反应的离子方程式
;
(3)如图所示,D跟B形成的离子化合物的化学式为 ;鉴别该离子化合物是否为晶体,最可靠的科学方法是 ,该离子化合物晶体的密度为ag·cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是 cm3(只要求列出算式)。
【解析】在前36号元素中,符合周期表中1—18列中的第8列元素的是铁,即E是铁,则D是Ca。根据D跟B形成离子化合物晶胞结构可判断,该离子化合物是DB2,则B是F或Cl。因为B和C属同一主族,且原子序数前者小于后者,所以B只能是F,C是Cl,A与其他4种元素既不在同一周期又不在同一族,所以A是H。
(1)HF属于分子晶体,由于HF中含有氢键,所以HF的沸点高于氯化氢的。
(2)氯气溶于水生成盐酸和次氯酸。
(3)鉴别离子化合物是否为晶体,最可靠的科学方法是射线衍射法。在该晶胞中含有的该离子是8×1/8+6×1/2=4,则F-是8,所以晶胞的体积是(8b+4c)/a NA。
查看习题详情和答案>>
(8分)有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1)A2B2的电子式为____________。
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。
在b电极上发生的反应可表示为:PbO2+4H++SO +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g / cm3)变为______mol /L。
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g / cm3)变为______mol /L。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为____________________________________。
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池(图乙),则在该原电池工作时,石墨一极发生的反应可以表示为______________________________。
(8分)有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1)A2B2的电子式为____________。
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。

在b电极上发生的反应可表示为:PbO2+4H++SO +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g / cm3)变为______mol
/L。
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g / cm3)变为______mol
/L。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为____________________________________。

(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池(图乙),则在该原电池工作时,石墨一极发生的反应可以表示为______________________________。
查看习题详情和答案>>