摘要: 二氧化硫使品红褪色的原因:
网址:http://m.1010jiajiao.com/timu3_id_354146[举报]
 二氧化硫和氯气是中学化学中的常见气体,探究二者的制法和性质是十分重要的课题.
二氧化硫和氯气是中学化学中的常见气体,探究二者的制法和性质是十分重要的课题.(1)实验室可由多种途径制取SO2.
途径Ⅰ:Na2SO3固体与较浓的硫酸(约70%)反应制取;
途径Ⅱ:铜与浓硫酸加热制取.
如果要在实验室制取SO2,选用上述两种方法中的
途径I
途径I
(填“途径Ⅰ”或“途径Ⅱ”)更合理,你的理由是制备等量的二氧化硫消耗的硫酸少
制备等量的二氧化硫消耗的硫酸少
(答出一点就可).(2)如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置.
已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
装置B、C、D的作用分别是:
B
向上排空气收集氯气
向上排空气收集氯气
;
C
安全瓶作用:防止D中的液体倒吸进入集气管B中
安全瓶作用:防止D中的液体倒吸进入集气管B中
;D
吸收尾气,防止氯气扩散到空气中污染环境
吸收尾气,防止氯气扩散到空气中污染环境
.(3)某同学设计用如下装置探究二氧化硫、氯气的化学性质.
通过控制弹簧夹a、b,向装置A中分别通入不同气体,请完成如下问题:
①若关闭b,打开a,若X为品红溶液,则A中的现象为:
品红溶液红色褪色
品红溶液红色褪色
,说明二氧化硫具有漂白性
漂白性
性.②若关闭a,打开b,若X为紫色石蕊试液,则A中的现象为:
溶液紫色先变红,后褪色
溶液紫色先变红,后褪色
,原因是氯气与水反应生成的酸使紫色变为红色,同时生成的HClO具有漂白性,使溶液红色褪去
氯气与水反应生成的酸使紫色变为红色,同时生成的HClO具有漂白性,使溶液红色褪去
.③若同时打开a、b,且通入的气体体积比为1:1,若X为紫色石蕊试液,则A中的现象为
溶液由紫色变为红色
溶液由紫色变为红色
,与②现象不同的原因是Cl2+SO2+2H2O=2HCl+H2SO4
Cl2+SO2+2H2O=2HCl+H2SO4
(书写相应的化学方程式).|
有关二氧化硫的说法错误的是 | |
A. |
SO2通入Na2CO3或NaHCO3溶液能发生反应 |
B. |
SO2能使品红溶液褪色是因它的氧化性 |
C. |
给已被SO2褪色的品红溶液用酒精灯加热,可恢复原来的红色 |
D. |
SO2和O2混合后在有催化剂存在的条件下加热,可生成三氧化硫 答案:B |
(2013?临沂三模)无水氯化铝是一种重要的化工原料,利用明矾石[K2SO4?Al2(SO4)3?2Al2O3?6H2O]制备无水氯化铝的流程如下:
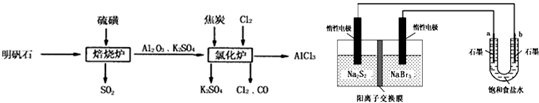
(1)焙烧炉中产生的SO2直接排放到空气中会形成酸雨,若某地酸雨的pH为4.6,在空气中放置一段时间后,pH变为4.0,其原因为
(2)氯化炉中发生的主要反应为:2Al2O3(s)+6Cl2(g)?4AlCl3(g)+3O2(g)△H>0.反应达平衡时,加焦炭能使平衡向正反应方向移动,理由是
(3)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染.试设计简单实验检验二者是否恰好完全反应.(简要描述实验步骤、现象和结论)
仪器自选,可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(4)工业上利用如下装置制备氯气:已知左侧原电池的工作原理为:2Na2S2+NaBr3
Na2S4+3NaBr
①用惰性电极电解饱和食盐水的化学方程式为
②如图所示原电池放电时,电池中的Na+向
③该原电池工作一段时间后,测得左槽中Na+物质的量由a mol变为b mol,则电解池中b电极上得到的气体在标准状况下的体积为
查看习题详情和答案>>

(1)焙烧炉中产生的SO2直接排放到空气中会形成酸雨,若某地酸雨的pH为4.6,在空气中放置一段时间后,pH变为4.0,其原因为
酸雨中的弱酸亚硫酸被氧化为强酸硫酸,使溶液中的c(H+)增大,pH减小
酸雨中的弱酸亚硫酸被氧化为强酸硫酸,使溶液中的c(H+)增大,pH减小
;(用必要的文字简述).(2)氯化炉中发生的主要反应为:2Al2O3(s)+6Cl2(g)?4AlCl3(g)+3O2(g)△H>0.反应达平衡时,加焦炭能使平衡向正反应方向移动,理由是
焦炭可消耗产物中的氧气,使c(O2)变小;且放出热量,温度升高,导致平衡向正反应方向移动
焦炭可消耗产物中的氧气,使c(O2)变小;且放出热量,温度升高,导致平衡向正反应方向移动
.(3)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染.试设计简单实验检验二者是否恰好完全反应.(简要描述实验步骤、现象和结论)
取少量溶液,向其中加入品红溶液,若品红溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应
取少量溶液,向其中加入品红溶液,若品红溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应
.仪器自选,可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(4)工业上利用如下装置制备氯气:已知左侧原电池的工作原理为:2Na2S2+NaBr3
| ||
①用惰性电极电解饱和食盐水的化学方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
②如图所示原电池放电时,电池中的Na+向
右槽
右槽
(填“左槽”或“右槽”)移动.左槽中发生的电极反应式为2S22--2e-=S42-
2S22--2e-=S42-
.③该原电池工作一段时间后,测得左槽中Na+物质的量由a mol变为b mol,则电解池中b电极上得到的气体在标准状况下的体积为
11.2(a-b)
11.2(a-b)
L(不考虑气体的损失).实验室制乙烯时,常因温度过高而发生副反应,使部分乙醇与浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和碳黑。
(1)请用下图编号为①②③④的装置设计一个实验,以验证上述反应混合气体中含有CO2,SO2和水蒸气。 用装置的编号表示装置的连接顺序(按产物气流从 左到右的顺序):___→____→___ →____
(1)请用下图编号为①②③④的装置设计一个实验,以验证上述反应混合气体中含有CO2,SO2和水蒸气。 用装置的编号表示装置的连接顺序(按产物气流从 左到右的顺序):___→____→___ →____

(2)实验时,装置①中C瓶的现象是____________,原因是____________。B瓶中的现象是____________;B瓶溶液的作用是____________。 若A瓶中品红溶液不褪色,说明_______________。
(3)装置③中加的固体药品是____________,以验证混合气体中有________________。装置②中盛放的溶液是________________,以验证混合气体中的________________。
(4)装置①在整套装置中所放位置的理由是____________________。
查看习题详情和答案>>
(3)装置③中加的固体药品是____________,以验证混合气体中有________________。装置②中盛放的溶液是________________,以验证混合气体中的________________。
(4)装置①在整套装置中所放位置的理由是____________________。
实验室制乙烯时,常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。
(1)请用下图中编号为①②③④的装置设计一个实验,以验证上述混合气体中含CO2、SO2和水蒸气。用装置的编号表示装置的连接顺序(按产物气流从左到右):________→________→________→________。

(2)实验时装置①中A瓶的现象是_________,原因是_________。B瓶中的现象是_________,B瓶溶液的作用是_________。若C瓶中品红溶液不褪色,说明_________。
(3)装置③中加的固体药品是_________,以验证混合气体中有_________。装置②中盛的溶液是_________,以验证混合气体中的_________。
(4)装置①在整套装置中所放位置的理由是__________________。
查看习题详情和答案>>