摘要:21.A.B.C.D.E均为常见的分子或离子.它们都具有10个电子.A是有五个 原子核的离子.它们之间的关系如下:.B+E=2D.D与酸性氧化物 和碱性氧化物均反应.则A的符号为 .B的符号为 . E的电子式为 .实验室制取C的化学方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_353964[举报]
 A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:(1)若A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液,E溶于NaOH溶液的离子方程式是
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
;工业上冶炼A的化学反应方程式是2NaCl(熔融)
2Na+Cl2↑
| ||
2NaCl(熔融)
2Na+Cl2↑
.
| ||
(2)若C是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式是
CaC2+2H2O→C2H2↑+Ca(OH)2
CaC2+2H2O→C2H2↑+Ca(OH)2
;1mol C完全燃烧生成液态水时放热1300kJ,则C完全燃烧的热化学方程式是2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJ?mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJ?mol-1
.A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是Ca(HCO3)2
Ca(HCO3)2
.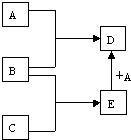 已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).请回答:
已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).请回答:(1)若A为Fe,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体Fe3O4,E常温常压下为无色无味的液体.则B的分子式为
(2)若A为Cl2,B为Fe,C为常见的酸,且C的组成中含有与A相同的元素.则构成非金属单质A的原子结构示意图为
A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则:该反应的反应方程式为 ,检验D中阴离子的方法是 .
(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行.写出反应的离子方程式 ; .
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的化学式(写两种) 、 写出生成E的一个离子方程式 .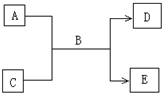
查看习题详情和答案>>
(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则:该反应的反应方程式为 ,检验D中阴离子的方法是 .
(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行.写出反应的离子方程式 ; .
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的化学式(写两种) 、 写出生成E的一个离子方程式 .

A、B、C、D、E均为中学化学常见的10电子粒子。已知,M(A)>M(B),
C是一种重要的化工原料。下图表示在1L的密闭容器中,一定条件下X、Y、C三种气体因发生反应而导致的物质的量随时间的变化情况。
回答下列问题。
(1)写出B的电子式 。
(2)写出FG的离子方程式 。
(3)根据题图写出相关的化学方程式 。(用化学式表示)
(4)下表为一定条件下平衡混合物中C的体积分数(C%)。分析数据可知,表中a的取值范围是 。
(5)根据题图和题表分析,25 min ~ 40 min内曲线发生变化的原因可能是 (填选项代号,下同);50 min ~ 65 min曲线发生变化的原因可能是 。
A.降低温度 B.增加C的物质的量 C.加了催化剂 D.缩小容器体积
(6)工业上合成C的温度一般选择在500℃左右,主要原因是 。
查看习题详情和答案>>