摘要:8.元素X和Y元素周期素中处于相邻周期.两种元素原子的质子数之和为21.Y元素原 子的核外电子数比X元素原子的核外电子数多5.则下列叙述不正确的是: A.X和Y两元素形成的化合物在熔融状态下电解可以得到两元素的单质 B.Y元素的单质不能和金属氧化物反应 C.X和Y能构成一种阴离子.这种阴离子与过量H+反应可以转变为Y元素的阳离子 D.X元素的一种单质能效地吸收太阳光线中的紫外线
网址:http://m.1010jiajiao.com/timu3_id_353825[举报]
元素X和Y元素周期素中处于相邻周期,两种元素原子的质子数之和为21,Y元素原子的核外电子数比X元素原子的核外电子数多5.则下列叙述不正确的是
- A.X和Y两元素形成的化合物既可以和强酸反应,也可以和强碱反应
- B.Y元素的单质不能盐酸反应
- C.X的离子和Y的离子核外电子排布完全相同
- D.X元素的一种单质能有效地吸收太阳光线中的紫外线
X元素和Y元素在周期表中处于相邻周期,两种元素原子的质子数之和为21,Y元素原子的核外电子数比X元素多5,则下列叙述中,不正确的是( )
A.电解Y的氯化物的水溶液可以制得Y元素的单质
B.Y元素的最高价氧化物的水化物在水中可以电离出四种离子
C.X和Y能构成一种阴离子,这种阴离子与过量的H+反应可以转变为Y元素的阳离子
D.X元素的一种单质能有效地吸收太阳光中的紫外线
查看习题详情和答案>>有X、Y、Z、W四种短周期元素,原子序数依次增大.X的阳离子就是一个质子.Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体.Y原子的最外层电子数是次外层电子数的2倍.请回答: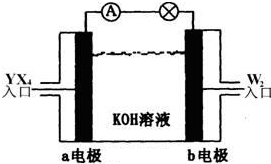
(1)Z2的电子式为
 ,Y的原子结构示意图为
,Y的原子结构示意图为
 ,YW2的结构式为
,YW2的结构式为
(2)将YX4、W2按上图所示通入某燃料电池中,则两极的电极方程式分别为:
a电极:
(3)已知在120℃、101kPa下,0.5mol X2在W2中完全燃烧时,释放出120.9kJ的热量,该反应的热化学方程式为
(4)Y和Z结合可生成一种超硬物质,本身耐磨损,抗腐蚀,则该物质属于
查看习题详情和答案>>

(1)Z2的电子式为




O=C=O
O=C=O
.(2)将YX4、W2按上图所示通入某燃料电池中,则两极的电极方程式分别为:
a电极:
CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
,b电极:O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
.若有16gW2参加反应,转移的电子数是2NA或1.204×1024
2NA或1.204×1024
.(3)已知在120℃、101kPa下,0.5mol X2在W2中完全燃烧时,释放出120.9kJ的热量,该反应的热化学方程式为
H2(g)+1/2 O2(g)═H2O(g)△H=-241.8kJ?mol-1
H2(g)+1/2 O2(g)═H2O(g)△H=-241.8kJ?mol-1
.(4)Y和Z结合可生成一种超硬物质,本身耐磨损,抗腐蚀,则该物质属于
原子
原子
晶体,该晶体中各粒子均满足8电子稳定结构,则化学式为C3N4
C3N4
.有X、Y、Z、W四种短周期元素,原子序数依次增大。X的阳离子就是一个质子。Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层电子数的2倍。请回答:
(1)Z2的电子式为 ,Y的原子结构示意图为 ,YW2的结构式为 。
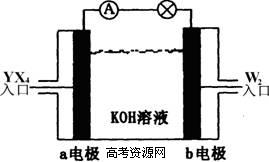
(2)将YX4、W2按上图所示通入某燃料电池中,则两极的电极方程式分别为:
a电极: ,b电极: 。若有16gW2参加反应,转移的电子数是 。
(3)已知在120℃、101kPa下, 0.5mol X2在W2中完全燃烧时,释放出120.9kJ的热量,该反应的热化学方程式为 。
(4)Y和Z结合可生成一种超硬物质,本身耐磨损,抗腐蚀,则该物质属于 晶体,该晶体中各粒子均满足8电子稳定结构,则化学式为 。
查看习题详情和答案>>