摘要: A.B.C.D四种短周期元素,原子序数依次增大.它们的单质在一定条件下都能与水反应.A与水反应的产物都是气体,1molB与水反应产生0.5mol气体F,1molC与水反应产生0.5mol气体E,E.F相化合生成水,D与水反应生成两种酸.则 (1)B单质与水反应的化学方程式为 (2)C与D所形成的化合物.其晶体的微粒间以 相结合.一个D的微粒周围最 近距离上有 个C的微粒.A与D所形成的化合物.其晶体的微粒以 相结合. (3)四种元素中.最高价氧化物的水化物酸性最强的是
网址:http://m.1010jiajiao.com/timu3_id_353378[举报]
 A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.(1)C元素在周期表中的位置
第三周期、第 VIIA族
第三周期、第 VIIA族
.(2)A元素与水反应的离子方程式是
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式
Cl2+Na2S=2NaCl+S↓
Cl2+Na2S=2NaCl+S↓
.(4)BD2和C2均具有漂白性,二者的漂白原理
不同
不同
.(填“相同”或“不同”)(5)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:3H2+N2
 2NH3△H=-92.4kJ?mol-1
2NH3△H=-92.4kJ?mol-1①当合成氨反应达到平衡后,改变某一外界条件 (不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.图中t1时引起平衡移动的条件可能是
加压
加压
,其中表示平衡混合物中NH3的含量最高的一段时间是t2-t3
t2-t3
.②温度为T℃时,将2a molH2和a molN2放入0.5L 密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为
| 4 |
| a2 |
| 4 |
| a2 |
A、B、C、D四种短周期元素原子序数依次增大,A元素原子的价电子排列为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2.C、D的电离能数据如下(kJ?mol-1):
(1)化合价是元素的一种性质.由C、D的电离能数据判断,C通常显
(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供
(5)如图所示晶胞中,阳离子与阴离子的个数为
查看习题详情和答案>>
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
+2
+2
价,D显+3
+3
价;(2)某单质甲分子与化合物AB分子中电子总数相等,则甲分子中包含
1
1
个σ键,2
2
个π键;(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应.根据下表数据,说明AB比甲活泼的原因是
断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼
断裂C≡O中的一个π键消耗的能量是273kJ/mol,断裂N≡N中的一个π键消耗的能量是523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼
.| 单键 | 双键 | 叁键 | ||
| AB | 键能(kJ?mol-1) | 357.7 | 798.9 | 1071.9 |
| 甲 | 键能(kJ?mol-1) | 154.8 | 418.4 | 941.7 |
 (4)E能与AB形成配合物,其中E提供
(4)E能与AB形成配合物,其中E提供空轨道
空轨道
,AB提供孤对电子
孤对电子
.(5)如图所示晶胞中,阳离子与阴离子的个数为
3:1
3:1
.A、B、C、D四种短周期元素,原子序数依次增大,A、C同主族,C、D同周期,B原子最外层电子数是最内层电子数的3倍.A、B可形成A2B和A2B2两种液态化合物,B、C也可形成C2B和C2B2两种固态化合物.C+具有与氖原子相同核外电子排布.D原子最外层电子数比B原子最外层电子数多一个电子,根据以上条件,判断:
(1)四种元素分别是(写元素符号) A
(2)用电子式写出A2B化合物的形成过程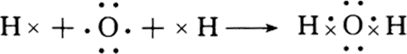
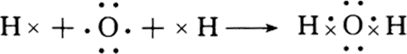 ; 用电子式写出C2B化合物的形成过程
; 用电子式写出C2B化合物的形成过程
 ;
;
(3)A2B2中加少量MnO2反应的化学方程式
查看习题详情和答案>>
(1)四种元素分别是(写元素符号) A
H
H
BO
O
CNa
Na
DCl
Cl
(2)用电子式写出A2B化合物的形成过程
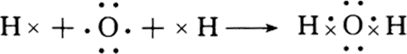
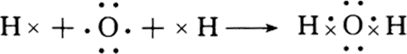


(3)A2B2中加少量MnO2反应的化学方程式
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;C2B2与CO2反应的化学方程
| ||
2Na2O2+2CO2═2Na2CO3+O2↑
2Na2O2+2CO2═2Na2CO3+O2↑
.A、B、C、D四种短周期元素的原子序数依次增大,A元素的气态氢化物与A元素的最高价氧化物对应的水化物能反应生成盐;B、C、D同周期,它们的最高价氧化物对应的水化物两两之间都能反应生成盐和水,B和D可组成化合物BD.回答下列问题:
(1)A元素的气态氢化物的结构式为:
 .D的最高价氧化物对应水化物的化学式:
.D的最高价氧化物对应水化物的化学式:
(2)在工业上常用
(3)C、D组成的化合物溶于水的离子方程式:
(4)B、C最高价氧化物对应的水化物在溶液中反应的离子方程式为:
查看习题详情和答案>>
(1)A元素的气态氢化物的结构式为:


HClO4
HClO4
.(2)在工业上常用
电解
电解
法制备单质C(填金属的冶炼方法)(3)C、D组成的化合物溶于水的离子方程式:
Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
 Al(OH)3+3H+
Al(OH)3+3H+Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
. Al(OH)3+3H+
Al(OH)3+3H+(4)B、C最高价氧化物对应的水化物在溶液中反应的离子方程式为:
Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.
(1)C元素在周期表中的位置
(2)A元素与水反应的离子方程式是
(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式
(4)BD2和C2均具有漂白性,二者的漂白原理
(5)B元素的单质在不同的条件下可以与O2发生一系列反应:
B(s)+O2=BO2(g);△H=-296.8kj?mol-1
2BD2(s)+O2(g) 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1
则1mol BO3(g)若完全分解成B(s),反应过程中的热效应为
(6)氢氧燃料电池能量转化率高,具有广阔的发展前景.如图(1)所示,电池中正极的电极反应式为
(7)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol

①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图(2)所示.图中t1时引起平衡移动的条件可能是
②温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为
.
查看习题详情和答案>>
(1)C元素在周期表中的位置
第三周期,第VIIA族
第三周期,第VIIA族
.(2)A元素与水反应的离子方程式是
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
.(3)写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的化学方程式
Cl2+Na2S=2NaCl+S↓
Cl2+Na2S=2NaCl+S↓
.(4)BD2和C2均具有漂白性,二者的漂白原理
不同
不同
.(填“相同”或“不同”)(5)B元素的单质在不同的条件下可以与O2发生一系列反应:
B(s)+O2=BO2(g);△H=-296.8kj?mol-1
2BD2(s)+O2(g)
 2BO3(g);△H=-196.6kJ?mol-1
2BO3(g);△H=-196.6kJ?mol-1则1mol BO3(g)若完全分解成B(s),反应过程中的热效应为
△H=+395.1kJ/mol
△H=+395.1kJ/mol
.(6)氢氧燃料电池能量转化率高,具有广阔的发展前景.如图(1)所示,电池中正极的电极反应式为
O2+2H20+4e-=4OH-
O2+2H20+4e-=4OH-
.(7)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g)
 2NGH3(g);△H=-92.4kJ/mol
2NGH3(g);△H=-92.4kJ/mol
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图(2)所示.图中t1时引起平衡移动的条件可能是
加压
加压
.其中表示平衡混合物中NH3的含量最高的一段时间是t2-t3
t2-t3
.②温度为T℃时,将2a molH2和a molN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该反应的平衡常数为
| 4 |
| a2 |
| 4 |
| a2 |