网址:http://m.1010jiajiao.com/timu3_id_353334[举报]
同主族元素的单质及其化合物在性质上有许多相似之处.如硫化物类似于氧化物,也有酸性、碱性的差异;氧化性与还原性的区别,也能发生类似于氧化物的许多变化.
根据上述规律,试写出下列反应的化学方程式.
(1)K2S+CS2________;
(2)K2S+As2S5________;
(3)Na2S2+SnS2________.
查看习题详情和答案>>根据上述叙述,完成下列反应的化学方程式:
(1)Na2S+As2S5![]() (2)Na2S2+SnS
(2)Na2S2+SnS![]()
查看习题详情和答案>>
同主族元素的单质及其化合物在性质上有许多相似之处。硫化物类似于氧化物,也有酸性与碱性之分和氧化性与还原性之分,也能发生类似于氧化物与氧化物之间的反应。例如:Na2O+CO2══Na2CO3;Na2S+CS2═Na2CS3(硫代碳酸钠)
根据上述叙述,完成下列反应的化学方程式:
(1)Na2S+As2S5![]() (2)Na2S2+SnS
(2)Na2S2+SnS![]()
查看习题详情和答案>>
(1)金属镁有许多重要的用途,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:


上述2种结构中均存在配位键,把你认为是配位键的用“→”标出.
(2)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是
(3)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
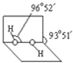 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取(5)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化关系:

①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键.
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2![]() Cl+Cl ②Cl+H2
Cl+Cl ②Cl+H2![]() HCl+H ③H+Cl2
HCl+H ③H+Cl2![]() HCl+Cl……
HCl+Cl……
反应②中形成的化合物的电子式为__________________;反应③中被破坏的化学键属于__________________键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与相邻元素的原子半径从大到小的顺序是__________________ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第__________________周期__________________族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是__________________。
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如下图。由图推断:

①非金属性强的卤素,其单质分子的化学键__________________断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:__________________。
查看习题详情和答案>>