摘要:将一定量的CuO和木炭的混合物放入试管中加热至充分反应后.把残留物分为两 等分:在第一份中加入63%浓HNO3.当固体完全溶解时.消耗HNO3 17.6g;在第二份中加入2mol/L的稀HNO3.当固体完全溶解时.消耗HNO3 12.6g .求混合物中CuO和木炭各多少克?
网址:http://m.1010jiajiao.com/timu3_id_351917[举报]
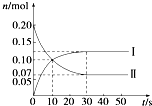 在容积为2L的密闭容器中,保持体系内温度800℃不变,将一定量的NO和O2混合发生反应:2NO+O2?2NO2,其中NO的物质的量(n)随时间(t)的变化关系如图所示.请回答下列问题.
在容积为2L的密闭容器中,保持体系内温度800℃不变,将一定量的NO和O2混合发生反应:2NO+O2?2NO2,其中NO的物质的量(n)随时间(t)的变化关系如图所示.请回答下列问题.(1)30s时反应达到平衡,用O2表示达到平衡过程的平均反应速率为
0.0022mol?L-1?s-1
0.0022mol?L-1?s-1
,图象中曲线II
II
(选填“Ⅰ”或“Ⅱ”)表示NO2的变化.由图象中曲线和数据变化,能否计算该温度下的平衡常数:不能
不能
(填“能”或“不能”).(2)若升高反应体系的温度,使反应重新达到平衡,此时体系中n(NO)=n(NO2),则该反应是
放
放
热反应(选填“吸”或“放”).(3)在800℃时,若缩小容器的体积,达新平衡时n(NO)
<
<
(选填“>”、“=”或“<”)0.07mol,NO的转化率增大
增大
(选填“增大”、“不变”或“减小”).(4)上述800℃时的反应达到平衡时测得放出热量a kJ.试写出在此条件下NO与氧气反应的热化学方程式
2NO(g)+O2(g)?2NO2(g)△H=-15.4a kJ?mol-1
2NO(g)+O2(g)?2NO2(g)△H=-15.4a kJ?mol-1
.1、(1)化学反应:I2+2S2O32-=2I-+S4O62-常用于精盐中碘含量测定.某同学利用该反应探究浓度对反应速率的影响.实验时均加入1mL淀粉溶液做指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择
①1mL 0.01mol?L-1的碘水 ②1mL 0.001mol?L-1的碘水
③4mL 0.01mol?L-1的Na2S2O3溶液 ④4mL 0.001mol?L-1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O32-)=
2、合成氨所需的氢气可用煤和水作原料经多步反应制得,其中某一步反应为:
CO(g)+H2O(g)?CO2(g)+H2(g)△H<0
200℃时,该反应的平衡常数为
,该温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质浓度(mol?L-1)变化如下表所示:
(1)5min达到平衡时,CO2的浓度为:
(2)欲提高CO的转化率,下列措施中可行的是
a.增加压强 b.降低温度 c.体积不变,再充入CO
d.更换催化剂 e.体积不变,再充入H2O
(3)若5min~10min只改变了某一条件,所改变的条件是:
(4)若某温度下,此反应的平衡常数为1,则该温度
查看习题详情和答案>>
②③④
②③④
(填序号).①1mL 0.01mol?L-1的碘水 ②1mL 0.001mol?L-1的碘水
③4mL 0.01mol?L-1的Na2S2O3溶液 ④4mL 0.001mol?L-1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O32-)=
8.33×10-4mol/(L?s)
8.33×10-4mol/(L?s)
.(结果保留三位有效数字)2、合成氨所需的氢气可用煤和水作原料经多步反应制得,其中某一步反应为:
CO(g)+H2O(g)?CO2(g)+H2(g)△H<0
200℃时,该反应的平衡常数为
| 1 |
| 2.25 |
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
0.004mol/L
0.004mol/L
;CO的平衡转化率为40%
40%
.(2)欲提高CO的转化率,下列措施中可行的是
be
be
(填字母).a.增加压强 b.降低温度 c.体积不变,再充入CO
d.更换催化剂 e.体积不变,再充入H2O
(3)若5min~10min只改变了某一条件,所改变的条件是:
增大水蒸气的浓度
增大水蒸气的浓度
;该条件所改变的量是:增大0.01mol/L
增大0.01mol/L
.(4)若某温度下,此反应的平衡常数为1,则该温度
小于
小于
200℃.(填“大于”、“等于”或“小于”).Ⅰ、铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛.
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为:
.其电极均由石墨材料做成,则电解时不断消耗的电极是 (填“阴极”或“阳极”).
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材
表面形成氧化膜,阳极反应式为 .
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,则负极的电极反应式为 ,正极附近溶液的pH (填“变大”、“不
变”或“变小”).
Ⅱ、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.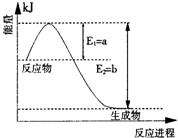
(1)图是在一定温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出合成氨的热化学反应方程式: (△H的数值用含字母a、b的代数式表示).
(2)工业合成氨的反应为
N2(g)+3H2(g)
2NH3(g).
在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 .
A.增大压强 B.增大反应物的浓度 C.使用催化剂 D.降低温度
Ⅲ、铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:
3FeS2+8O2
6SO2+Fe3O4,有3mol FeS2参加反应,转移 mol电子;
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式: .
查看习题详情和答案>>
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为:
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材
表面形成氧化膜,阳极反应式为
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,则负极的电极反应式为
变”或“变小”).
Ⅱ、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.

(1)图是在一定温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出合成氨的热化学反应方程式:
(2)工业合成氨的反应为
N2(g)+3H2(g)
| 催化剂 |
| 高温高压 |
在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是
A.增大压强 B.增大反应物的浓度 C.使用催化剂 D.降低温度
Ⅲ、铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:
3FeS2+8O2
| ||
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式: