摘要:(B)下列反应在210℃达到平衡: PCl5(气) PCl3(气)+Cl2(气)-Q1 K=1 ① CO(气)+Cl2(气) COCl2(气)+Q2 K=5x104 ② COCl2+Cl2(气)-Q2 ③ (1)根据反应①的平衡常数K表达式,下列等式必定成立的是 (a)[PCl5]=[PCl3]=[Cl2]=1 (b)[PCl5]=[PCl3][Cl2]=1 (c)[PCl5]=[PCl3][Cl2] 反应②和反应③的平衡常数K表达式 (填"相同"或"不同"); (2)降低Cl2浓度,反应③的K值 (填"增大"."减小"或"不变"); (3)要使反应①和反应②的K值相等,应采取的措施是 . (a)反应①.反应②同时升高温度 (b)反应①.反应②同时降低温度 (c)反应①降低温度,反应②维持在210℃
网址:http://m.1010jiajiao.com/timu3_id_351504[举报]
(2012?丹东模拟)二甲醚(CH3OCH3)被称为21世纪的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)═CH3OH(g)△H1=-90.7kJ?mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g)△H3=-41.2kJ?mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为
A.加入某物质作催化剂
B.加入一定量CO
C.反应温度降低
D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,则5min内CO的平均反应速率为
(3)催化反应室中总反应3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)的△H=
(4)二甲醚的燃烧热为1455kJ?mol-1,则二甲醚燃烧的热化学方程式为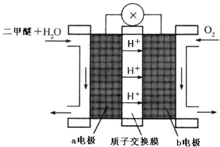
(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示.写出a电极上发生的电极反应式
查看习题详情和答案>>
①CO(g)+2H2(g)═CH3OH(g)△H1=-90.7kJ?mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-23.5kJ?mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g)△H3=-41.2kJ?mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为
B C
B C
.A.加入某物质作催化剂
B.加入一定量CO
C.反应温度降低
D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,则5min内CO的平均反应速率为
0.1mol/(L?min)
0.1mol/(L?min)
;若反应物的起始浓度分别为:c(CO)=4mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2mol/L,a=5.4
5.4
mol/L.(3)催化反应室中总反应3CO(g)+3H2(g)═CH3OCH3(g)+CO2(g)的△H=
-246.1 kJ?mol-1
-246.1 kJ?mol-1
;830℃时反应③的K=1.0,则在催化反应室中反应③的K>
>
1.0(填“>”、“<”或“=”).(4)二甲醚的燃烧热为1455kJ?mol-1,则二甲醚燃烧的热化学方程式为
CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455 kJ?mol-1
CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455 kJ?mol-1
.
(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示.写出a电极上发生的电极反应式
CH3OCH3+3H2O-12e-=2CO2+12H+
CH3OCH3+3H2O-12e-=2CO2+12H+
.一定温度下,向1.0L密闭容器中加入0.60molX(g),发生反应X(g)?Y(s)+2Z(g)△H>0测得反应物X浓度与反应时间的数据如下表
(1)3min时用Z表示的平均反应速率v(Z)= .
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是 .由此规律推出反应在6min时反应物的浓度a为 mol?L-1.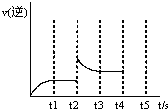
(3)反应的逆反应速率随时间变化的关系如图,t2时改变了某一种条件,改变的条件可能是 、 (填写两顶)
(4)下列哪些情况表明容器中已达平衡状态 (填字母序号)
A.容器体积一定时气体密度不再变化
B.反应的平衡常数不再变化
C.容器中气体的平均相对分子质量不随时间而变化
D.Y的物质的量不再发生变化
E.Z的生成速率等于X的消耗速率的2倍.
查看习题详情和答案>>
| 反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
| c(X)/(mol?L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是

(3)反应的逆反应速率随时间变化的关系如图,t2时改变了某一种条件,改变的条件可能是
(4)下列哪些情况表明容器中已达平衡状态
A.容器体积一定时气体密度不再变化
B.反应的平衡常数不再变化
C.容器中气体的平均相对分子质量不随时间而变化
D.Y的物质的量不再发生变化
E.Z的生成速率等于X的消耗速率的2倍.
阅读下列信息:
(Ⅰ)“R-CH=CH2”型烯烃(R为烷基或氢原子)可发生下列反应:
R-H=CH2+CO+H2
R-CH2-CH2-CHO.
(Ⅱ)由烃M可以制得一种用于汽车、家电的高分子涂料F,其生产流程图如下所示:

在相同条件下M的密度是氢气的21倍,其在氧气中完全燃烧生成二氧化碳和水的质量之比为22:9,B的相对分子质量比D的相对分子质量小16,A和B均能与银氨溶液反应,B的分子式为C3H4O,E的分子式为C7H12O2.
(1)F在一定条件下能与下列试剂发生反应的是
A.酸性高锰酸钾溶液
B.氢氧化钠溶液,加热
C.氢气/催化剂,加热
D.氯化铁溶液
(2)写出下列反应的化学方程式:
①M→B:
②C+D→E:
(3)E有多种同分异构体,写出一种含有三个甲基且与E为同类物质的同分异构体的结构简式:
查看习题详情和答案>>
(Ⅰ)“R-CH=CH2”型烯烃(R为烷基或氢原子)可发生下列反应:
R-H=CH2+CO+H2
| 催化剂 |
(Ⅱ)由烃M可以制得一种用于汽车、家电的高分子涂料F,其生产流程图如下所示:

在相同条件下M的密度是氢气的21倍,其在氧气中完全燃烧生成二氧化碳和水的质量之比为22:9,B的相对分子质量比D的相对分子质量小16,A和B均能与银氨溶液反应,B的分子式为C3H4O,E的分子式为C7H12O2.
(1)F在一定条件下能与下列试剂发生反应的是
D
D
(填序号).A.酸性高锰酸钾溶液
B.氢氧化钠溶液,加热
C.氢气/催化剂,加热
D.氯化铁溶液
(2)写出下列反应的化学方程式:
①M→B:
2CH3CH=CH2+O2
2CH2=CH-CHO+2H2O
| 催化剂 |
| △ |
2CH3CH=CH2+O2
2CH2=CH-CHO+2H2O
;| 催化剂 |
| △ |
②C+D→E:
CH2=CH-COOH+CH3CH2CH2CH2OH
CH2=CH-COOCH2CH2CH2CH3+H2O
| 浓硫酸 |
| △ |
CH2=CH-COOH+CH3CH2CH2CH2OH
CH2=CH-COOCH2CH2CH2CH3+H2O
.| 浓硫酸 |
| △ |
(3)E有多种同分异构体,写出一种含有三个甲基且与E为同类物质的同分异构体的结构简式:
CH2=CH-COOC(CH3)3等
CH2=CH-COOC(CH3)3等
. 二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
二甲醚(CH3OCH3)具有优良的燃烧性能,被称为21世纪的“清洁能源”.一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:①CO(g)+2H2(g )?CH3OH(g);△H1=90.7 kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H2=23.5 kJ?mol-1
③CO(g)+H2O?(g)CO2(g)+H2(g);△H3=41.2 kJ?mol-1
(1)-步法合成二甲醚的总反应可表示为3CO(g)+3H2(g)CH3OCH3(g)+CO2(g),该反应的AH=
-246.1kJ/mol
-246.1kJ/mol
.平衡常数表达式为K=
| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
K=
.| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
(2)另一种合成二甲醚的方法称为“二步法”,该工艺为让反应①和反应②分别在不同的反应器中进行,无反应③发生,而“一步法”的反应③的发生提高了CH3OCH3的产率,原因是
反应③消耗了反应②中的水,使得②的平衡正向移动,从而提高了甲醚的产率
反应③消耗了反应②中的水,使得②的平衡正向移动,从而提高了甲醚的产率
.(3)由CO2加氢直接合成二甲醚可以消除过度CO2排放对环境的影响.当在合成反应器中加入碳氢比[n(CO2)/n(H2)]为1:3的混合气体,在一定条件下反应得到二甲醚和水蒸气,实现了CO2的减排目的.该反应的反应方程式为
2CO2+6H2
CH3OCH3+3H2O
| ||
2CO2+6H2
CH3OCH3+3H2O
; 判断该反应在一定温度下,体积恒定的密闭容器中下列不能作为达到化学平衡状态的依据是
| ||
A
A
A.容器的密度不变
B.容器内压强保持不变
C,平均摩尔质量保持不变
D.单位时间内消耗2mol CO2,同时消耗1mol二甲醚
(4)以二甲醚为燃料的燃料电池工作原理如图所示:则正极为
B
B
(填A极或B极),写出A电极反应式CH3OCH3+3H2O-12e-=2CO2+12H+
CH3OCH3+3H2O-12e-=2CO2+12H+
.甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)??CH3OH(g).

(1)分析该反应并回答下列问题:
①平衡常数表达式为K=
.
②下列各项中,不能够说明该反应已达到平衡的是
A、恒温、恒容条件下,容器内的压强不发生变化
B、一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C、一定条件下,CO、H2和CH3OH的浓度保持不变
D、一定条件下,单位时间内消耗2mol CO,同时生成1mol CH3OH
(2)如图1是该反应在不同温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H
②T1和T2温度下的平衡常数大小关系是K1
③若容器容积不变,下列措施可增加甲醇产率的是
A、升高温度
B、将CH3OH(g)从体系中分离
C、使用合适的催化剂
D、充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图2所示.
①该电池工作时,b口通入的物质为
②该电池正极的电极反应式为:
③工作一段时间后,当6.4g甲醇完全反应生成CO2时,有
查看习题详情和答案>>

(1)分析该反应并回答下列问题:
①平衡常数表达式为K=
| c(CH3OH) |
| c(CO)?c(H2)2 |
| c(CH3OH) |
| c(CO)?c(H2)2 |
②下列各项中,不能够说明该反应已达到平衡的是
D
D
(填序号).A、恒温、恒容条件下,容器内的压强不发生变化
B、一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
C、一定条件下,CO、H2和CH3OH的浓度保持不变
D、一定条件下,单位时间内消耗2mol CO,同时生成1mol CH3OH
(2)如图1是该反应在不同温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H
<
<
0(填“>”、“<”或“=”).②T1和T2温度下的平衡常数大小关系是K1
>
>
K2(填“>”、“<”或“=”).③若容器容积不变,下列措施可增加甲醇产率的是
B
B
.A、升高温度
B、将CH3OH(g)从体系中分离
C、使用合适的催化剂
D、充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图2所示.
①该电池工作时,b口通入的物质为
CH3OH
CH3OH
,c口通入的物质为O2
O2
.②该电池正极的电极反应式为:
O2+4e-+4H+=2H2O
O2+4e-+4H+=2H2O
.③工作一段时间后,当6.4g甲醇完全反应生成CO2时,有
1.2
1.2
NA个电子转移.