摘要:25.在一定温度下.有1mol N2气体和3mol H2气体发生下列反应: N2(g)+3H2(g)2NH3(g),△H<0 (1)若在相同温度下.分别在1L定压密闭容器中和1L定容容器中反应: 哪个容器中的反应先达到平衡? 答: 哪个容器中的N2的转化率高? 答: (2)若在上述定压密闭容器中.反应已达到平衡时.再加入0.5摩氩气.则N2的转化率会起什么变化?正反应速度与原平衡相比.有无变化.简答理由. (3)若在1升定容容器中.上述反应达到平衡时.平衡混和物中N2.H2.NH3的物质的量分别为A.B.C摩.仍维持原温度.用x.y.z分别表示开始时N2.H2.NH3的加入量(mol).应满足的条件是: ①若x=0.y=0.则z= . ②若x=0.75.则y应为 mol.z应为 mol. ③x.y.z应满足的一般条件是 .
网址:http://m.1010jiajiao.com/timu3_id_351474[举报]
 (2013?河西区一模)肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.请按要求回答下列问题:
(2013?河西区一模)肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.请按要求回答下列问题:(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:


(2)实验室用两种固体制取NH3的反应化学方程式为
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
| ||
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
.
| ||
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为
2NH3+NaClO=N2H4+NaCl+H2O
2NH3+NaClO=N2H4+NaCl+H2O
.(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为
N2H4+4OH--4e-=N2+4H2O
N2H4+4OH--4e-=N2+4H2O
.(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
<
<
0(填“>”、“<”或“=”).②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
| n(NH3) |
| n(CO2) |
c(NH3)增大,平衡正向移动
c(NH3)增大,平衡正向移动
.图中A点处,NH3的平衡转化率为42%
42%
.(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)?2NH3(g),测得甲容器中H2的平衡转化率为40%.
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
逆向
逆向
(填“正向或“逆向”)移动.②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为
甲=乙=丙
甲=乙=丙
.
氨是重要的化工原料,合成氨是哈伯1905年发明的.2001年希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池中,H2和N2在电极上合成氨.此法的转化率大为提高.已知:N2 (g)+3H2 (g)?2NH3(g)△H<0.请回答下列问题:
(1)电解法合成氨可以使用水做电解液吗? ,为什么? .
(2)若合成氨反应容器的容积为2L,开始充入3mol H2和1mol N2 反应达到平衡时气体的压强变为原来的
,则氮气的转化率为 .该反应的化学平衡常数的表达式为 ,升高温度,平衡常数将 .(填增大、减少或不变);增大反应容器的体积,再达到平衡时,混合气的平均分子量将 .(填增大、减少或不变).
(3)在一定条件下氨可与其他物质反应生成尿素〔CO(NH2)2〕,已知30g尿素在高温高压下分解生成11.2LNH3(标况)、5.6LCO2和一定量的三聚氰胺分子(三聚氰胺的相对分子质量为126).不法分子曾在低蛋白含量的奶粉中加入三聚氰胺来提高奶粉中的蛋白质含量,导致许多婴幼儿肾结石.写出三聚氰胺的分子式为 ,其化学反应方程式为 . 三聚氰胺分子中有一个六元环,一个三聚氰胺分子可分解生成三个分子A,则A的结构式是 .
查看习题详情和答案>>
(1)电解法合成氨可以使用水做电解液吗?
(2)若合成氨反应容器的容积为2L,开始充入3mol H2和1mol N2 反应达到平衡时气体的压强变为原来的
| 7 | 8 |
(3)在一定条件下氨可与其他物质反应生成尿素〔CO(NH2)2〕,已知30g尿素在高温高压下分解生成11.2LNH3(标况)、5.6LCO2和一定量的三聚氰胺分子(三聚氰胺的相对分子质量为126).不法分子曾在低蛋白含量的奶粉中加入三聚氰胺来提高奶粉中的蛋白质含量,导致许多婴幼儿肾结石.写出三聚氰胺的分子式为
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法.请回答下列问题:
(1)450℃时,往一个2L的密闭容器中充入2.6mol H2和1mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
①5min内,消耗N2的平均反应速率为______,此条件下该反应的化学平衡常数K=______;反应达到平衡后,若往平衡体系中加入H2、N2和NH3各2mol,此时该反应的v(N2)正______v(N2)逆(填写“>”、“=”或“<”=).
②下列各项能作为判断该反应达到化学平衡状态的依据是______(填序号字母)
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v(N2)正=3v(H2)逆 C.容器内压强保持不变
D.混合气体的密度保持不变 E.容器内混合气体的平均分子量不变
③若改变某一条件,达新平衡时n(H2)=1.60mol,下列说法正确的是______.
A.平衡一定正向移动 B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度 D.可能是缩小了容器的体积
(2)450℃时,在另一密闭容器中进行上述合成氨的反应,各物质的起始浓度和平衡浓度如下表所示:
请回答:
①各物质的平衡浓度可能是______.
A.c=0.5mol/L B.b=0.5mol/L C.c=0.4mol/L D.a=0.3mol/L
②a的取值范围是:______.
③请用数学表达式表示下列量之间的关系:
(I)a与b的关系:______.
(Ⅱ)a、b、c的关系:______.
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水可发生下列反应:2N2(g)+6H2O(l)?4NH3(g)+3O2(g),此反应的△S______0(填“>”、“<”或“=”),△H=______.(已知:H2的燃烧热为285.8kJ/mol)
查看习题详情和答案>>
(1)450℃时,往一个2L的密闭容器中充入2.6mol H2和1mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol?L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②下列各项能作为判断该反应达到化学平衡状态的依据是______(填序号字母)
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v(N2)正=3v(H2)逆 C.容器内压强保持不变
D.混合气体的密度保持不变 E.容器内混合气体的平均分子量不变
③若改变某一条件,达新平衡时n(H2)=1.60mol,下列说法正确的是______.
A.平衡一定正向移动 B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度 D.可能是缩小了容器的体积
(2)450℃时,在另一密闭容器中进行上述合成氨的反应,各物质的起始浓度和平衡浓度如下表所示:
| N2 | H2 | NH3 | |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
①各物质的平衡浓度可能是______.
A.c=0.5mol/L B.b=0.5mol/L C.c=0.4mol/L D.a=0.3mol/L
②a的取值范围是:______.
③请用数学表达式表示下列量之间的关系:
(I)a与b的关系:______.
(Ⅱ)a、b、c的关系:______.
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水可发生下列反应:2N2(g)+6H2O(l)?4NH3(g)+3O2(g),此反应的△S______0(填“>”、“<”或“=”),△H=______.(已知:H2的燃烧热为285.8kJ/mol)
查看习题详情和答案>>
 (2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题:
(2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题:(1)在298K时,将10mol N2和30mol H2放入合成塔中,为何放出的热量小于924kJ?
该反应为可逆反应,10molN2和30molH2不可能完全反应,所以放出的热量小于10×10×92.4kJ=924kJ
该反应为可逆反应,10molN2和30molH2不可能完全反应,所以放出的热量小于10×10×92.4kJ=924kJ
.(2)如图一在一定条件下,将1mol N2与3mol H2混合于一个10L密闭容器中,反应达到A平衡时,混合气体中氨占25%,试回答:
①N2的转化率αA为
40%
40%
.②在状态A时,平衡常数KA=
| 0.082 |
| 0.06×0.183 |
| 0.082 |
| 0.06×0.183 |
>
>
KB(填“>”、“<”或“=”)(3)图二是实验室模拟工业法合成氨的简易装置.简述检验有氨气生成的方法
用湿润的红色石蕊试纸放在导管口处,若试纸变蓝,说明有氨气生成
用湿润的红色石蕊试纸放在导管口处,若试纸变蓝,说明有氨气生成
.在1998年希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨.其实验装置如图.阴极的电极反应式N2+6e-+6H+=2NH3
N2+6e-+6H+=2NH3
.已知:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
(1)450℃时,往一个2L的密闭容器中充入2. 6mol H2和1mol N2, 反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L—1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②下列各项能作为判断该反应达到化学平衡状态的依据是__________(填序号字母)
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v(N2)正=3v(H2)逆 C.容器内压强保持不变
D.混合气体的密度保持不变 E.容器内混合气体的平均分子量不变
③若改变某一条件,达新平衡时n(H2)="1.60mol" ,下列说法正确的是_____________。
A.平衡一定正向移动 B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度 D.可能是缩小了容器的体积
(2)450℃时,在另一密闭容器中进行上述合成氨的反应,各物质的起始浓度和平衡浓度如下表所示:
| | N2 | H2 | NH3 |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
①各物质的平衡浓度可能是_______________.
A.c="0.5mol/L " B.b="0.5mol/L " C.c="0.4mol/L " D.a=0.3mol/L
②a的取值范围是:_______________.
③请用数学表达式表示下列量之间的关系:
(I)a与b的关系:_______________。
(Ⅱ)a、b、c的关系:_______________。
(3) 根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水可发生下列反应:2N2(g)+6H2O(l)
 4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“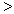 ”、 “
”、 “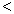 ”或“=”), △H=_____________。
”或“=”), △H=_____________。(已知:H2的燃烧热为285.8 kJ/mol) 查看习题详情和答案>>