摘要:89. CH3CHCOOH NH2
网址:http://m.1010jiajiao.com/timu3_id_350470[举报]
(2013?淮南一模)从废钒催化剂(主要成分有V2O5,VOSO4,K2SO4,SiO2等)中回收V2O5的一种生产流程示意图如下,请回答下列问题:
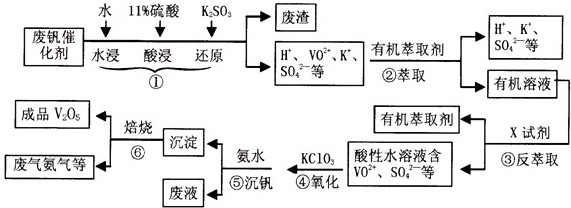
(1)步骤①中废渣的主要成分是
(2)实验室中进行萃取分液操作时,注入萃取剂,充分振荡,将分液漏斗于铁圈上静置,当液体分层后,接下来的操作是
(3)②③的变化过程可简化为(下式R表示VO 2+,HA表示有机萃取剂)
R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
为提高②中萃取百分率,应采取的措施是
(4)请完成④中反应的离子方程式:
(5)25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH值为
(6)该工艺流程中,可以循环利用的物质有
查看习题详情和答案>>

(1)步骤①中废渣的主要成分是
SiO2
SiO2
,③中X试剂为H2SO4
H2SO4
;(均填化学式)(2)实验室中进行萃取分液操作时,注入萃取剂,充分振荡,将分液漏斗于铁圈上静置,当液体分层后,接下来的操作是
打开分液漏斗瓶塞(或瓶塞凹槽对准瓶口小孔);当分液面接近(或略超过)活塞处时关闭活塞;上层液体从分液漏斗上口倒入另一烧杯中
打开分液漏斗瓶塞(或瓶塞凹槽对准瓶口小孔);当分液面接近(或略超过)活塞处时关闭活塞;上层液体从分液漏斗上口倒入另一烧杯中
;(3)②③的变化过程可简化为(下式R表示VO 2+,HA表示有机萃取剂)
R2(SO4)n(水层)+2nHA(有机层)?2RAn(有机层)+nH2SO4(水层)
为提高②中萃取百分率,应采取的措施是
加入碱中和硫酸使平衡正移
加入碱中和硫酸使平衡正移
;(4)请完成④中反应的离子方程式:
1
1
ClO3-+6
6
VO2++6
6
H-+=6
6
VO3++1Cl-
1Cl-
+3H2O
3H2O
(5)25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如表
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
1.7-1.8
1.7-1.8
;(6)该工艺流程中,可以循环利用的物质有
氨气 有机萃取剂
氨气 有机萃取剂
.哈雷彗星上碳的两种同位素12C和13C的原子个数比为65:1.而地球上12C和13C的原子个数比为89:1,地球上碳元素的原子相对质量是12.011,那么哈雷彗星上碳元素的原子相对质量是( )
查看习题详情和答案>>
(2010?天津一模)次氯酸盐最大的用途是漂白和消毒.这类漂白剂氧化能力是以“有效氯”的含量来标志.“有效氯”的含量定义为:从HI中氧化出相同量的I2所需Cl2的质量与指定化合物的质量之比,常以百分数表示.请问纯LiClO的“有效氯”为( )
查看习题详情和答案>>
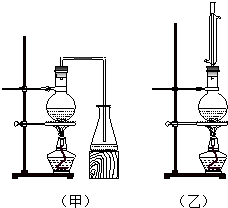 实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用.
实验室制取乙酸丁酯的实验装置有如图甲、乙两种装置可供选用.制备乙酸丁酯所涉及的有关物质的物理性质见下表:
| 乙酸 | 1-丁醇 | 乙酸丁酯 | |
| 熔点(℃) | 16.6 | -89.5 | -73.5 |
| 沸点(℃) | 117.9 | 117 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 可溶 (9g/100g水) |
微溶 |
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简式)
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,写出两种可行的方法:
①
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是
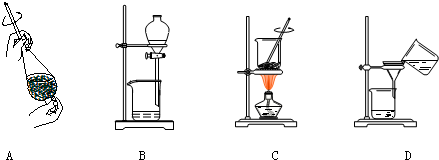
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器.使用分液漏斗前必须
(1)质量都为a g的镁和铝,物质的量之比为
(2)在含有35.8g Na2CO3和NaHCO3混合物的溶液中加入200mL 某浓度的盐酸,恰好完全反应,生成8.96L CO2(标准状况).则原溶液中有
(3)已知Cu3P中P为-3价,在反应 11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4 中:
①被氧化的P和被还原的P的物质的量之比为
②当有8mol H2O参加反应,上述反应转移的电子数目为
查看习题详情和答案>>
9:8
9:8
;将它们分别放入适量的盐酸溶液中恰好完全反应,则消耗的HCl的物质的量之比为3:4
3:4
.(2)在含有35.8g Na2CO3和NaHCO3混合物的溶液中加入200mL 某浓度的盐酸,恰好完全反应,生成8.96L CO2(标准状况).则原溶液中有
0.1
0.1
mol Na2CO3,盐酸的物质的量浓度为2.5
2.5
mol/L.(3)已知Cu3P中P为-3价,在反应 11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4 中:
①被氧化的P和被还原的P的物质的量之比为
6:5
6:5
.②当有8mol H2O参加反应,上述反应转移的电子数目为
10NA
10NA
个.