摘要:1.常见气体的检验 气体 常用的反应和现象 注意问题 空气 木条能燃.但不能使带火星的木条复燃 NO2 N2O气体也能“助燃 O2 能使带火星的木条复燃 H2 点燃火焰呈浅蓝色.只生成H2O.不纯者点燃有爆鸣声 ①点燃可燃性气体时一定要验纯 ②用玻璃导管点燃有时看不到蓝色火焰.因Na+燃烧有黄色火焰 CO 点燃火焰呈蓝色.生成物只有CO2 H2S 点燃火焰呈蓝色.不完全燃烧生成硫,遇Pb(Ac)2.或Pb(NO3)2湿试纸变黑.有臭鸡蛋味 CH4 点燃火焰呈浅蓝色.生成CO2或水,不使溴水或KMnO4酸性溶液褪色 ③遇到多种可燃性气体除点燃外.还要利用特征或燃烧产物的性质加以区别(如H2S有臭鸡蛋味.也能使溴水褪色或KMnO4酸性溶液褪色.但有硫沉淀). C2H4 点燃火焰较高.有微黑烟,使溴水或酸性KMnO4溶液褪色 C2H2 点燃.火焰明亮有较浓黑烟,使溴水或酸性KMnO4溶液褪色 NH3 使湿润红色石蕊试纸变蓝.遇蘸浓盐酸的玻璃棒有白烟 在空气中不燃.但在纯氧中可燃. 4NH3+3O2(纯)=2N2+6H2O NO 开瓶盖或遇空气立即变成红棕色 NO在空气中不存在 NO2 红棕色.但溶于水为无色溶液.遇AgNO3溶液无沉淀,使蓝色石蕊试纸变红 两者都能使KI-淀粉试纸变蓝.不能用它区别(O3也能) Br2蒸气 溶于水成橙黄色溴水.与AgNO3溶液出浅黄色沉淀,使蓝色石蕊试纸变红 Cl2 黄绿色.使KI-淀粉湿试纸变蓝,使品红湿试纸褪色 与石灰水无沉淀 SO2 使澄清石灰水出现白色沉淀后澄清.使品红溶液褪色.加热后恢复原色.使酸性KMnO4溶液或溴水褪色 ①SO2具有刺激性气体.CO2无气味.它们都可使石蕊由蓝变红.SO2更显著.不用此鉴别 ②SO2和CO2通入石灰水的现象一样 CO2 使澄清石灰水出现白色沉淀后澄清.但不使品红溶液KMnO4酸性溶液溴水等溶液褪色 HCl 使湿润蓝色石蕊试纸变红.遇蘸氨水的玻璃棒出白烟.遇AgNO3溶液白色沉淀 HI.HBr气体同HCl.但遇AgNO3溶液分别出AgI, AgBr的黄色及浅黄色沉淀 N2 不发生上述所有情况或现象 只有镁能在其中点燃生成Mg3N2
网址:http://m.1010jiajiao.com/timu3_id_349889[举报]
常见的治疗缺铁性贫血的方法是服用补铁药物,市场上一种常见的补铁药物的商品名称是:速力菲,正式名称是:琥珀酸亚铁薄膜片,为棕黄色薄膜衣片,除去薄膜衣后显暗黄色,药片中Fe2+的含量约为34.0%~36.0%.该药片在水和乙醇中的溶解度不大.某学校化学实验小组为了检测“速力菲”药片中Fe2+的存在,设计了如下几组理论实验设计方案:
Ⅰ.甲组方案:
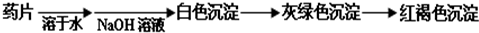
(提示:白色的Fe(OH)2在空气中会迅速变成灰绿色,最后变成红褐色)
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果.分析甲组实验失败的可能原因:
Ⅱ.乙组同学在参考书上查得如下资料:
①人体胃液中有大量盐酸,能溶解多种物质.
②H2O2不稳定,光照、加热和微量杂质会促使其分解;H2O2中氧元素为-1价,它既有氧化性又有还原性.
他们认真思考了甲组实验失败的原因,模拟药服用后在人体中溶解的变化过程,重新设计并完成下列实验:
乙组方案:
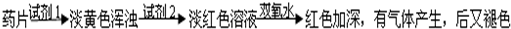
(1)试剂1为:
(2)加入试剂2后,溶液显淡红色的原因是:
(3)加双氧水后,红色加深的原因是:
Ⅲ.丙组同学对乙组实验中最后红色褪去的现象产生了浓厚的兴趣,欲探究其褪色的原因.根据粒子的组成,他们认为有两种可能原因:①[Fe(SCN)]2+中的三价铁被还原为亚铁;②
请你对其中一种可能进行实验验证:
实验方案(用文字叙述):
根据预期现象判断结论:
查看习题详情和答案>>
Ⅰ.甲组方案:
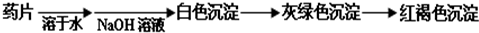
(提示:白色的Fe(OH)2在空气中会迅速变成灰绿色,最后变成红褐色)
甲组同学按照设计的方案完成实验,但遗憾的是他们没有得到预期的实验结果.分析甲组实验失败的可能原因:
该药片在水中溶解度不大,少量溶解后的溶液中几乎不存在Fe2+离子,所以得不到预期的实验现象.
该药片在水中溶解度不大,少量溶解后的溶液中几乎不存在Fe2+离子,所以得不到预期的实验现象.
.Ⅱ.乙组同学在参考书上查得如下资料:
①人体胃液中有大量盐酸,能溶解多种物质.
②H2O2不稳定,光照、加热和微量杂质会促使其分解;H2O2中氧元素为-1价,它既有氧化性又有还原性.
他们认真思考了甲组实验失败的原因,模拟药服用后在人体中溶解的变化过程,重新设计并完成下列实验:
乙组方案:
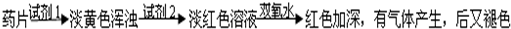
(1)试剂1为:
盐酸
盐酸
,试剂2为:KSCN溶液
KSCN溶液
;(2)加入试剂2后,溶液显淡红色的原因是:
在溶液形成过程中有少量Fe2+已经氧化成Fe3+离子,滴加KSCN溶液后,Fe3+离子与SCN-离子结合成浓度较小的红色[Fe(SCN)]2+络离子.
在溶液形成过程中有少量Fe2+已经氧化成Fe3+离子,滴加KSCN溶液后,Fe3+离子与SCN-离子结合成浓度较小的红色[Fe(SCN)]2+络离子.
;(3)加双氧水后,红色加深的原因是:
加入的H2O2能将Fe2+氧化为Fe3+,导致溶液中Fe3+浓度增大,[Fe(SCN)]2+络离子浓度也随之增大,所以红色加深.
加入的H2O2能将Fe2+氧化为Fe3+,导致溶液中Fe3+浓度增大,[Fe(SCN)]2+络离子浓度也随之增大,所以红色加深.
.根据氧化还原反应中化合价变化情况,试写出在酸性条件下Fe2+与双氧水反应的离子方程式:H2O2+2Fe2++2H+=2Fe3++2H2O
H2O2+2Fe2++2H+=2Fe3++2H2O
.Ⅲ.丙组同学对乙组实验中最后红色褪去的现象产生了浓厚的兴趣,欲探究其褪色的原因.根据粒子的组成,他们认为有两种可能原因:①[Fe(SCN)]2+中的三价铁被还原为亚铁;②
SCN-被双氧水氧化
SCN-被双氧水氧化
.请你对其中一种可能进行实验验证:
实验方案(用文字叙述):
在褪色后溶液中加入FeCl3溶液或在褪色后溶液中加入KSCN溶液
在褪色后溶液中加入FeCl3溶液或在褪色后溶液中加入KSCN溶液
.根据预期现象判断结论:
在褪色后溶液中加入FeCl3溶液现象:变红色结论:褪色原因是因为①;不变红色结论:褪色原因是因为②
或在褪色后溶液中加入KSCN溶液
现象:变红色结论:褪色原因是因为②;不变红色结论:褪色原因是因为①
或在褪色后溶液中加入KSCN溶液
现象:变红色结论:褪色原因是因为②;不变红色结论:褪色原因是因为①
在褪色后溶液中加入FeCl3溶液现象:变红色结论:褪色原因是因为①;不变红色结论:褪色原因是因为②
或在褪色后溶液中加入KSCN溶液
现象:变红色结论:褪色原因是因为②;不变红色结论:褪色原因是因为①
.或在褪色后溶液中加入KSCN溶液
现象:变红色结论:褪色原因是因为②;不变红色结论:褪色原因是因为①
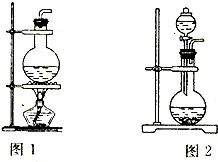 依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.
依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.(1)实验前需检查装置的气密性.图2装置检查气密性的方法是
(2)氨气的实验室制法常见的有三种,其中一种制法是将生石灰和浓氨水混合,此法应该选用
 依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.
依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为多种,这是其中的两套.
(1)实验前需检查装置的气密性.图2装置检查气密性的方法是______.
(2)氨气的实验室制法常见的有三种,其中一种制法是将生石灰和浓氨水混合,此法应该选用______装置(填“图1”或“图2”)该实验中有大量氨气逸出的原因是______.
查看习题详情和答案>>
某些化学反应可表示为:A+B═C+D+H2O(未配平,条件略).请回答:
(1)若A是常见金属,且A的合金用量最大,A与B的浓溶液在常温时发生钝化,但A与B的稀溶液反应产生无色气体并能迅速转化为红棕色.请写出过量的A与B的稀溶液反应的化学方程 ,若要检验反应后的溶液中含有的金属阳离子,其方法是 (写出操作、现象和结论).
(2)若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式 .
(3)若A为黑色固体,C是黄绿色的单质气体,反应的化学方程式为 ;
若向100mL 12.0mol?L-1的B中加入足量的A固体并加热,充分反应后在标准状况下生成C的体积是 (填字母序号).
A.等于6.72L B.小于6.72L
C.等于13.44L D.大于6.72L小于13.44L
(4)已知炭和浓硫酸在加热时也符合上述反应式,某同学设计如下实验证明其产物:
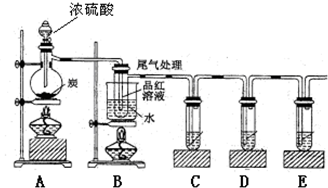
若证明有水生成,需要在A、B之间加装盛有 (填化学式)固体的干燥管;若证明生成CO2,C、D、E试管中分别需要盛放的试剂是 、 、 ;装置B可以探究SO2与品红作用的可逆性,请写出实验操作及现象 .
查看习题详情和答案>>
(1)若A是常见金属,且A的合金用量最大,A与B的浓溶液在常温时发生钝化,但A与B的稀溶液反应产生无色气体并能迅速转化为红棕色.请写出过量的A与B的稀溶液反应的化学方程
(2)若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式
(3)若A为黑色固体,C是黄绿色的单质气体,反应的化学方程式为
若向100mL 12.0mol?L-1的B中加入足量的A固体并加热,充分反应后在标准状况下生成C的体积是
A.等于6.72L B.小于6.72L
C.等于13.44L D.大于6.72L小于13.44L
(4)已知炭和浓硫酸在加热时也符合上述反应式,某同学设计如下实验证明其产物:

若证明有水生成,需要在A、B之间加装盛有
中学化学常见的物质A、B、C、D之间存在如下转化关系:A+B→C+D+H2O(没有配平).请按要求填空:
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体.C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是:______,鉴别这两种气体不能选用的试剂是______
a.BaCl2溶液 b.KMnO4溶液 c.品红溶液 d.酸化的Ba(NO3)2溶液
向500mL2mol/L的NaOH溶液中通入0.8mol无色无味的C气体,恰好完全反应,该反应的化学方程式是______.此时溶液中的离子按照浓度由大到小排列的顺序是______.
(2)若A为红色金属单质,与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成经棕色.若被还原的B物质的量为2mol时,产生C气体的体积是______ L(标况).将生成的红棕色气体通入一个烧瓶里,塞紧瓶塞后,将烧瓶浸入冰水中,烧瓶中气体的颜色变浅,请用化学方程式和必要的文字解释颜色变化的原因______.
(3)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质;D是漂白粉的成分之一.C发生水解反应的离子方程式是______
(4)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阴离子的方法是______(简述操作过程及结论).
查看习题详情和答案>>
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体.C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是:______,鉴别这两种气体不能选用的试剂是______
a.BaCl2溶液 b.KMnO4溶液 c.品红溶液 d.酸化的Ba(NO3)2溶液
向500mL2mol/L的NaOH溶液中通入0.8mol无色无味的C气体,恰好完全反应,该反应的化学方程式是______.此时溶液中的离子按照浓度由大到小排列的顺序是______.
(2)若A为红色金属单质,与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成经棕色.若被还原的B物质的量为2mol时,产生C气体的体积是______ L(标况).将生成的红棕色气体通入一个烧瓶里,塞紧瓶塞后,将烧瓶浸入冰水中,烧瓶中气体的颜色变浅,请用化学方程式和必要的文字解释颜色变化的原因______.
(3)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质;D是漂白粉的成分之一.C发生水解反应的离子方程式是______
(4)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阴离子的方法是______(简述操作过程及结论).