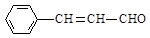摘要:22.(1) ,Ag++Br-=AgBr↓ .Br2.稀NaOH溶液.蒸馏水,分液漏斗.取少量最后一次洗液.加入稀HNO3.再加入AgNO3溶液.溶液不浑浊说明产品已洗净.(4)该反应是放热反应.反应物和Fe粉加入的量不适当.会使液溴挥发.挥发的液溴溶于水.生成HBr.与AgNO3反应生成AgBr沉淀.因而无法确定HBr是否与Br2取代反应的产物.Br2+H2O=HBr+HBrO HBr+AgNO3=AgBr↓+HNO3 (5)a是安全瓶.防止倒吸.b中试剂是苯或四氯化碳.装置Ⅱ的优点①控制反应进行.②防止倒吸 ③排除液溴的干扰 ④防止有害气体污染环境.
网址:http://m.1010jiajiao.com/timu3_id_349865[举报]
A.1 mol该有机物发生银镜反应能生成 1 mol Ag
B.1 mol该有机物最多能够与6 mol H2 发生加成反应
C.它与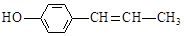 互为同分异构体
互为同分异构体
D.该有机物中所有原子可能在同一平面上
查看习题详情和答案>>
现有CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L—1的硫酸溶液50mL,恰好
完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量( )
A.1.6 ag B.(a-1.6)g C.(a-3.2)g D.ag
查看习题详情和答案>>
|
现有 CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L-1的硫酸溶液50 mL,恰好完全反应.若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量 | |
| [ ] | |
A. |
1.6 ag |
B. |
(a-1.6)g |
C. |
(a-3.2)g |
D. |
a g |
(2009?静安区一模)某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器).
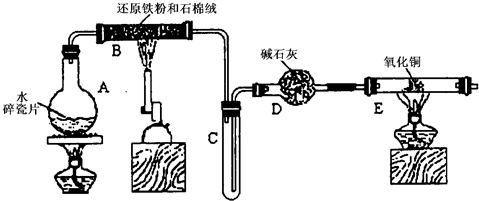
(1)仪器B的名称是
(2)B中发生反应的化学方程式是
(3)加热E以前要对装置中的气体验纯,方法是:收集一试管气体,然后
(4)已知有反应:Cu20+2H+→Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是
a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量.若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg.
①水中元素的物质的量之比可表示为n(H):n(0)=
②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为
.
查看习题详情和答案>>

(1)仪器B的名称是
石英管或硬质玻璃管
石英管或硬质玻璃管
,石棉绒的作用是增大铁与水蒸气接触面积,防止加热时固体喷入导管
增大铁与水蒸气接触面积,防止加热时固体喷入导管
.(2)B中发生反应的化学方程式是
3Fe+4H2O(g)
Fe3O4+H2
| ||
3Fe+4H2O(g)
Fe3O4+H2
.
| ||
(3)加热E以前要对装置中的气体验纯,方法是:收集一试管气体,然后
将试管口靠近酒精灯火焰,弱发出噗的声音,说明气体纯净;若发生尖锐爆鸣声,说明气体不纯
将试管口靠近酒精灯火焰,弱发出噗的声音,说明气体纯净;若发生尖锐爆鸣声,说明气体不纯
.(4)已知有反应:Cu20+2H+→Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是
bc
bc
(填序号)a.稀硝酸 b.稀硫酸 c.盐酸 d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量.若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg.
①水中元素的物质的量之比可表示为n(H):n(0)=
e-c-(b-d):
| b-d |
| 16 |
e-c-(b-d):
;若反应后E中除Cu外还含有另种还原产物Cu20,则该比值将| b-d |
| 16 |
无影响
无影响
(选填“偏大”“偏小”或“无影响”).②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为
| 16(d-a) |
| b-d |
| 16(d-a) |
| b-d |