摘要:某强酸性溶液中.含有大量的Fe2+.Ba2+.K+.则此溶液中不可能存在的离子是 A.MnO B.Fe3+ C.NO D.Cu2+
网址:http://m.1010jiajiao.com/timu3_id_34984[举报]
某强酸性溶液X可能含有Ba2+、Al3+、N
、Fe2+、Fe3+、C
、S
、S
、Cl-、N
、N
中的一种或几种,取该溶液进行连续实验,实验过程如下:
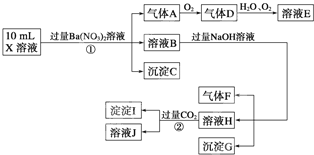
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
(2)沉淀I的化学式为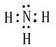
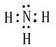 .
.
(3)写出反应②的离子方程式:
(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式
(5)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有
查看习题详情和答案>>
| H | + 4 |
| O | 2- 3 |
| O | 2- 3 |
| O | 2- 4 |
| O | - 2 |
| O | - 3 |

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
Al3+、NH4+、Fe2+、SO42-
Al3+、NH4+、Fe2+、SO42-
,不能确定是否含有的离子(M)是Fe3+、Cl-
Fe3+、Cl-
,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是取少量X溶液于试管中,加入几滴KSCN溶液不变红色则说明无Fe3+;或取少量B溶液少许于试管中,加几滴AgNO3溶液,若无白色沉淀说明无Cl-
取少量X溶液于试管中,加入几滴KSCN溶液不变红色则说明无Fe3+;或取少量B溶液少许于试管中,加几滴AgNO3溶液,若无白色沉淀说明无Cl-
.(2)沉淀I的化学式为
Al(OH)3
Al(OH)3
,气体F的电子式为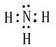
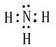
(3)写出反应②的离子方程式:
AlO2-+CO2+H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+H2O=Al(OH)3↓+HCO3-
.(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式
3ClO-+2Fe(OH)3+4OH-=3Cl-+FeO42-+5H2O
3ClO-+2Fe(OH)3+4OH-=3Cl-+FeO42-+5H2O
.(5)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有
Fe3+
Fe3+
.某强酸性溶液X可能含有Ba2+、A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-、NO2-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
(2)沉淀I的化学式为
 .
.
(3)写出生成A的离子方程式:
(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式
(5)1.0mol/L的E溶液与2.0mol/LF溶液等体积混合完全反反应后,溶液中各离子的浓度大小关系为
(6)假设测定A、F、I均为0.10mol,50mL X溶液中n(H+)=0.40mol,当沉淀C物质的量大于0.70mol时,溶液X中还一定含
查看习题详情和答案>>

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是
A13+、NH4+、Fe2+、SO42-
A13+、NH4+、Fe2+、SO42-
,不能确定是否含有的离子(M)是Fe3+Cl-
Fe3+Cl-
,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是取少量X溶液于试管中,加入几滴KSCN溶液,溶液不变红色则说明无Fe3+;或取少量B溶液于试管中,加入几滴AgNO3溶液,若无白色沉淀说明无Cl-
取少量X溶液于试管中,加入几滴KSCN溶液,溶液不变红色则说明无Fe3+;或取少量B溶液于试管中,加入几滴AgNO3溶液,若无白色沉淀说明无Cl-
.(2)沉淀I的化学式为
Al(OH)3
Al(OH)3
,气体F的电子式为

(3)写出生成A的离子方程式:
3Fe2++4H++NO3-═3Fe3++NO+2H2O
3Fe2++4H++NO3-═3Fe3++NO+2H2O
.(4)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式
3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O
3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O
.(5)1.0mol/L的E溶液与2.0mol/LF溶液等体积混合完全反反应后,溶液中各离子的浓度大小关系为
C(NH4+)>C(NO3-)>C(OH-)>C(H+)
C(NH4+)>C(NO3-)>C(OH-)>C(H+)
.(6)假设测定A、F、I均为0.10mol,50mL X溶液中n(H+)=0.40mol,当沉淀C物质的量大于0.70mol时,溶液X中还一定含
Fe3+
Fe3+
.某强酸性溶液X可能含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下:
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子是______,不能确定是否含有的离子(M)是______,若要确定该M(若不止一种,可任选一种)在溶液X中不存在,最可靠的化学方法是______.
(2)写出反应②的离子方程式:______.
(3)通常可以利用KClO在一定条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式______.
(4)假设测定A、F、I均为0.1mol,10mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有______.