网址:http://m.1010jiajiao.com/timu3_id_349725[举报]

请完成下列问题:?
(1)一个C60分子中有多少个五边形和多少个六边形??
(2)一个C60分子中有多少个C=C??
(3)已知C70分子的结构模型也遵循C60的那些规律,请确定C70分子结构中上述几项参数。?


C60的结构
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系遵循欧拉定理:
顶点数+面数-棱边数=2。
据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为30。
请回答下列问题:
(1)固体C60与金刚石相比较,熔点较高者应是_________,理由是:_____________________________________________________________________。
(2)试估计C60跟F2在一定条件下能否发生反应生成C60F60(填“可能”或“不可能”)_______________________,理由:__________________________________。
(3)通过计算,确定C60分子所含单键数为 _________________。
(4)C70分子也已制得,它的分子结构模型可以与C60同样考虑而推知。通过计算确定C70分子中五边形和六边形的数目。C70分子中所含五边形数为___________,六边形数为__________。
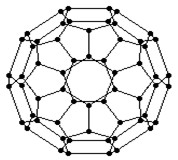
查看习题详情和答案>>1996年诺贝尔化学奖授予对发现C60有重大贡献的三位科学家。C60分子是形如球状的多面体,如右图,该结构的建立基于以下考虑:C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;碳与碳之间既有单键又有双键,每个碳原子仍然满足四个价键饱和;多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2。
请完成下列问题:
(1)一个C60分子中有多少个五边形和多少个六边形?
(2)一个C60分子中有多少个C=C?
(3)已知C70分子的结构模型也遵循C60的那些规律,请确定C70分子结构中上述几项参数。