摘要:在反应2X+5Y====4R+2M中.已知R和M的摩尔质量之比为22∶9.当2.6 g X与Y完全反应.生成4.4 g R.则在此反应中消耗Y和生成M的质量比为 A.26∶9 B.3∶1 C.40∶9 D.53∶9
网址:http://m.1010jiajiao.com/timu3_id_34954[举报]
X和Y在密闭容器中发生如下反应2X(g)+Y(g)═nZ(g)+2W(g),X和Y的起始浓度均为0.3mol?L-1,2分钟达平衡,W的浓度为0.1mol?L-1,Z的浓度为0.2mol?L-1,则:
(1)用X表示的反应速率为υ(X)=
(2)平衡时Y的浓度为C(Y)=
(3)n值为
查看习题详情和答案>>
(1)用X表示的反应速率为υ(X)=
0.05mol?L-1?min-1
0.05mol?L-1?min-1
;(2)平衡时Y的浓度为C(Y)=
0.25mol?L-1
0.25mol?L-1
;(3)n值为
4
4
.下列叙述与图象对应符合的是( )
A、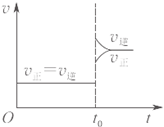 对于达到平衡状态的N2(g)+3H2(g)?2NH3(g),如图表示在t0时刻充入了一定的NH3,平衡逆向移动 | B、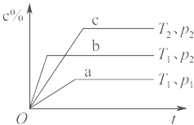 由如图可知p2>p1,T1>T2 | C、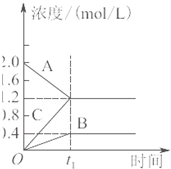 如图表示的方程式为2A?B+3C | D、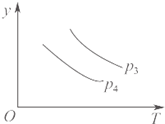 对于反应2X(g)+3Y(g)?2Z(g)△H<0,如图y轴可以表示Y的百分含量 |
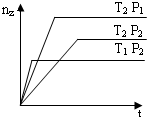 反应 2X(气)+Y(气)?2Z(气)+热量,在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应 2X(气)+Y(气)?2Z(气)+热量,在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )