摘要:(NH4)2PtCl6晶体受热完全分解,放出氮气和氯化氢气体.同时还生成金属铂和氯化铵.在这个反应中.若放出的N2是xmol.那么还原出的Pt是 ( ) A.x/2 mol B.2x mol C.2x/3 mol D.3x/2 mol
网址:http://m.1010jiajiao.com/timu3_id_348804[举报]
有一瓶澄清透明溶液,可能含有NH4+、Fe2+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、NO3-、Cl-中的一种或几种.取该溶液进行以下实验:
(1)溶液滴在蓝色石蕊试纸上,试纸呈红色;
(2)取部分溶液浓缩后加入铜片和浓硫酸共热,有红棕色气体生成;
(3)取少量溶液,加入硝酸酸化的氯化钡溶液,产生白色沉淀;
(4)将(3)中的沉淀滤出,滤液中加入硝酸银溶液,生成白色沉淀;
(5)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程先看到生成沉淀,随之沉淀部分溶解,并呈红褐色.
根据上述实验事实确定:在该溶液中肯定存在的离子是
查看习题详情和答案>>
(1)溶液滴在蓝色石蕊试纸上,试纸呈红色;
(2)取部分溶液浓缩后加入铜片和浓硫酸共热,有红棕色气体生成;
(3)取少量溶液,加入硝酸酸化的氯化钡溶液,产生白色沉淀;
(4)将(3)中的沉淀滤出,滤液中加入硝酸银溶液,生成白色沉淀;
(5)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程先看到生成沉淀,随之沉淀部分溶解,并呈红褐色.
根据上述实验事实确定:在该溶液中肯定存在的离子是
Fe3+、NO3-、Al3+、SO42-
Fe3+、NO3-、Al3+、SO42-
,肯定不存在的离子是HCO3-、Ba2+、Fe2+
HCO3-、Ba2+、Fe2+
,不能确定是否存在的离子是NH4+、C1-
NH4+、C1-
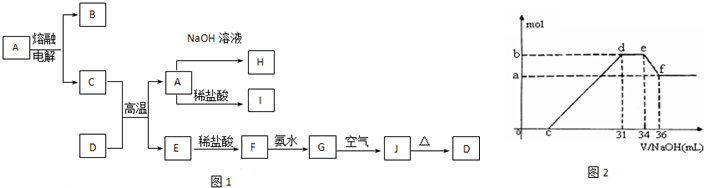
.A-J是中学化学中常见的物质,它们之间的转化关系如框图1所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.请回答下列问题:
(1)A的化学式为
(2)H溶液中通入过量的CO2,其反应的离子方程式是
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为
②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式
上述现象说明溶液中
③b与a的差值为
查看习题详情和答案>>
(1)A的化学式为
Al2O3
Al2O3
(2)H溶液中通入过量的CO2,其反应的离子方程式是
[Al(OH)4]-+CO2═Al(OH)3↓+HCO3-
[Al(OH)4]-+CO2═Al(OH)3↓+HCO3-
G→J的化学方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3
4Fe(OH)2+2H2O+O2═4Fe(OH)3
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为
H++OH-=H2O
H++OH-=H2O
.②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式
NH4++OH-=NH3?H2O
NH4++OH-=NH3?H2O
;上述现象说明溶液中
H+
H+
结合OHˉ的能力最强(填离子符号).③b与a的差值为
0.008mol
0.008mol
mol.
现有一瓶由Na+、NH4+、Cl-、NO3-、CO32-、SO42-、SO32-、OH-等离子中的某几种组成的混合物.用A、B、C三支试管,各取少量该混合液,分别进行如下实验:
(1)向试管A中滴加Ba(NO3)2溶液,有白色沉淀析出.
(2)向试管B中加入稀HNO3至溶液呈酸性,有无色气体冒出.继续加入AgNO3溶液或Ba(NO3)2溶液,均无沉淀生成.
(3)取试管C滴加几滴酚酞试液,溶液呈红色,再加入Cu片和浓H2SO4共热,一段时间后,试管口冒红棕色的气体.根据上述实验现象推断,下列说法正确的是( )
①原溶液中可能含有Na+,OH-,CO32-,NO3-;②一定不可能含有Cl-,NH4-,SO42-,SO32-;③原溶液中可能含有Cl-,CO32-,SO42-;④一定不可能含有NH4+,SO42-,CO32-.
(1)向试管A中滴加Ba(NO3)2溶液,有白色沉淀析出.
(2)向试管B中加入稀HNO3至溶液呈酸性,有无色气体冒出.继续加入AgNO3溶液或Ba(NO3)2溶液,均无沉淀生成.
(3)取试管C滴加几滴酚酞试液,溶液呈红色,再加入Cu片和浓H2SO4共热,一段时间后,试管口冒红棕色的气体.根据上述实验现象推断,下列说法正确的是( )
①原溶液中可能含有Na+,OH-,CO32-,NO3-;②一定不可能含有Cl-,NH4-,SO42-,SO32-;③原溶液中可能含有Cl-,CO32-,SO42-;④一定不可能含有NH4+,SO42-,CO32-.
查看习题详情和答案>>