摘要:13.用U型管电解滴有甲基橙指示剂的KNO3溶液.两极发生的现象是 ( ) A 阴阳极析出的气体体积比为1∶2 B 阴阳极析出的气体体积比为2∶1 C 通电一段时间后.阴极区甲基橙显黄色.阳极区甲基橙显橙色或红色 D 通电一段时间后.阴极区甲基橙显橙色或红色.阳极区甲基橙显黄色
网址:http://m.1010jiajiao.com/timu3_id_348722[举报]
如图甲所示,A、F为石墨电极,B、E为铁片电极.按要求回答下列问题:

(1)打开K2,闭合K1,B为
(2)打开K1,闭合K2,E为
(3)若往U型管中滴加酚酞,进行(1)、(2)操作时,
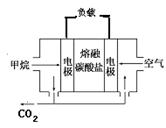
(4)若电源选用燃料电池,结构如图乙,以熔融碳酸盐为电解质(非水溶济,能够传导CO32-),电池工作时电解质组成保持稳定,通入甲烷的电极为
查看习题详情和答案>>

(1)打开K2,闭合K1,B为
负
负
极,A的电极反应为O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
,最终可观察到的现象是溶液中有红褐色沉淀生成
溶液中有红褐色沉淀生成
.(2)打开K1,闭合K2,E为
阴
阴
极,检验F极产生气体的方法是用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝
用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝
.该装置中发生反应的化学方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(3)若往U型管中滴加酚酞,进行(1)、(2)操作时,
A、E
A、E
极周围能变红(填A、B、E、或F).(4)若电源选用燃料电池,结构如图乙,以熔融碳酸盐为电解质(非水溶济,能够传导CO32-),电池工作时电解质组成保持稳定,通入甲烷的电极为
负
负
极,请写出正极反应的方程式2CO2+O2+4e-=2CO32-
2CO2+O2+4e-=2CO32-
,若在标况下消耗11.2L的甲烷,电解NaCl溶液产生的H2的物质的量为1.5
1.5
mol(假设燃料电池能量转化率为75%). Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:
Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:正极:
2O2+8H++8e-=4H2O
2O2+8H++8e-=4H2O
负极:
CH4+2H4O-8e-=CO2+8H+
CH4+2H4O-8e-=CO2+8H+
总反应:
CH4+2O4=CO2+2H2O
CH4+2O4=CO2+2H2O
Ⅱ、如图所示,A、F为石墨电极,B、E为铁片电极.
按要求回答下列问题.
(1)打开K2,合并K1.
①B为
负
负
极,A极的电极反应为:O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
②最终可观察到的现象是:
溶液中有红褐色沉淀生成
溶液中有红褐色沉淀生成
③涉及的两个主要的化学反应的化学方程式为:
2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3
(2)打开K1,合并K2.
①E为
阴
阴
极,F极的电极反应为:2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
②检验F极产生气体的方法是:
用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气
用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是
A、E
A、E
,原因是:(在下表中填写,可不填满)| 周围变红的电极代号(填字母) | 原因 |
A A |
O2+2H2O+4e-=4OH-,产生OH- O2+2H2O+4e-=4OH-,产生OH- |
E E |
2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) 2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) |
无 无 |
无 无 |
无 无 |
无 无 |
若X、Y两种元素在周期表中位于同一主族,其中一种为短周期元素,且两者相隔一个周期,并有m=n>0。在一定条件下有下列反应(未配平):Xm +Yn+H2O→HXO3+HY。请回答下列问题:
(1)该反应的还原剂的电子式为______________。
(2)配平上述化学方程式:_________________(用化学式表示)。
(3)若某化学反应如下:KX +Yn+H2O→KXO3+Xm+HY+KY(未配平),且KXO3和Xm的化学计量数均为1,则Yn的化学计量数为__________。标出电子转移的方向和数目:KX+Yn+H2O→ ______________
(4)已知:在反应中,若氧化反应和还原反应发生在同一分子中处于同一化合价的同种元素上,使该元素的原子(或离子)一部分被氧化,另一部分被还原,这种自身的氧化还原反应称为歧化反应。实验室模拟KXO3的制法如下
(1)该反应的还原剂的电子式为______________。
(2)配平上述化学方程式:_________________(用化学式表示)。
(3)若某化学反应如下:KX +Yn+H2O→KXO3+Xm+HY+KY(未配平),且KXO3和Xm的化学计量数均为1,则Yn的化学计量数为__________。标出电子转移的方向和数目:KX+Yn+H2O→ ______________
(4)已知:在反应中,若氧化反应和还原反应发生在同一分子中处于同一化合价的同种元素上,使该元素的原子(或离子)一部分被氧化,另一部分被还原,这种自身的氧化还原反应称为歧化反应。实验室模拟KXO3的制法如下

①在进行步骤I的实验时,有学生主张电解装置用U型管,有的学生主张用烧杯,你认为用哪种仪器更合适_________(填名称)。
②步骤I的阴极电极反应式为_____________________ (用化学式表示)。
③步骤I中由NaYO歧化生成NaYO3的离子方程式为__________________(用化学式表示)。
④步骤Ⅱ中向NaYO3溶液中加入粉末状的KY,搅拌后生成KYO3。在2 L 3 mol/L的NaYO3溶液中,至少需要加入_______mol KY粉末可将溶液中的YO3-沉淀至浓度变为0.1 mol/L[已知Ksp(KYO3)=0.366,计算结 果保留两位小数,加入KY粉末后溶液体积不变]。
查看习题详情和答案>>
②步骤I的阴极电极反应式为_____________________ (用化学式表示)。
③步骤I中由NaYO歧化生成NaYO3的离子方程式为__________________(用化学式表示)。
④步骤Ⅱ中向NaYO3溶液中加入粉末状的KY,搅拌后生成KYO3。在2 L 3 mol/L的NaYO3溶液中,至少需要加入_______mol KY粉末可将溶液中的YO3-沉淀至浓度变为0.1 mol/L[已知Ksp(KYO3)=0.366,计算结 果保留两位小数,加入KY粉末后溶液体积不变]。
(16分)如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题:
(1)打开K2,闭合K1,B为__________极,A的电极反应为______________,最终可观察到的现象是 。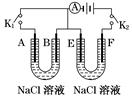
(2)打开K1,闭合K2,E为________极,检验F极产生气体的方法是 。
(3)若往U型管中滴加酚酞,进行(1)、(2)操作时, 极周围能变红(填A、B、E、或F,下同)。若滴加K3[Fe(CN)6]溶液,在 极周围溶液变为 色。
(4)若电源选用燃料电池,结构如图,以熔融碳酸盐为电解质(能够传导CO32-),电池工作时电解质组成保持稳定,请写出正极反应的方程式 ,若在标况下消耗11.2L的甲烷,电解NaCl溶液产生的H2的物质的量为 mol(假设燃料电池能量转化率为75%)。
xk