题目内容
 Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:
Ⅰ、写出甲烷燃料电池在酸性溶液中的电极反应和总电池反应:正极:
2O2+8H++8e-=4H2O
2O2+8H++8e-=4H2O
负极:
CH4+2H4O-8e-=CO2+8H+
CH4+2H4O-8e-=CO2+8H+
总反应:
CH4+2O4=CO2+2H2O
CH4+2O4=CO2+2H2O
Ⅱ、如图所示,A、F为石墨电极,B、E为铁片电极.
按要求回答下列问题.
(1)打开K2,合并K1.
①B为
负
负
极,A极的电极反应为:O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
②最终可观察到的现象是:
溶液中有红褐色沉淀生成
溶液中有红褐色沉淀生成
③涉及的两个主要的化学反应的化学方程式为:
2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3
(2)打开K1,合并K2.
①E为
阴
阴
极,F极的电极反应为:2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
②检验F极产生气体的方法是:
用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气
用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是
A、E
A、E
,原因是:(在下表中填写,可不填满)| 周围变红的电极代号(填字母) | 原因 |
A A |
O2+2H2O+4e-=4OH-,产生OH- O2+2H2O+4e-=4OH-,产生OH- |
E E |
2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) 2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) |
无 无 |
无 无 |
无 无 |
无 无 |
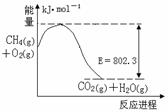
分析:Ⅰ、燃料电池中负极上燃料失电子和水反应生成二氧化碳和氢离子,正极上氧气得电子和氢离子反应生成水,据此写出正负极上电极反应式和电池反应式.
Ⅱ、(1)打开K2,合并K1,该装置是原电池,较活泼的金属铁作负极,石墨作正极,正极上氧气得电子和水反应生成氢氧根离子,铁发生吸氧腐蚀;负极上铁失电子生成亚铁离子,正极上生成氢氧根离子,亚铁离子和氢氧根离子 反应生成氢氧化亚铁沉淀,氢氧化亚铁易被氧化生成氢氧化铁,据此判断实验现象并写出反应方程式.
(2)该装置是电解池,F是阳极,E是阴极,阳极上氯离子放电,阴极上氯离子放电,写出相应的电极反应式;检验氯气用湿润的淀粉碘化钾试纸,能使湿润的淀粉碘化钾试纸变蓝就是氯气,否则不是.
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,电极周围能变红说明产生氢氧根离子,据此分析.
Ⅱ、(1)打开K2,合并K1,该装置是原电池,较活泼的金属铁作负极,石墨作正极,正极上氧气得电子和水反应生成氢氧根离子,铁发生吸氧腐蚀;负极上铁失电子生成亚铁离子,正极上生成氢氧根离子,亚铁离子和氢氧根离子 反应生成氢氧化亚铁沉淀,氢氧化亚铁易被氧化生成氢氧化铁,据此判断实验现象并写出反应方程式.
(2)该装置是电解池,F是阳极,E是阴极,阳极上氯离子放电,阴极上氯离子放电,写出相应的电极反应式;检验氯气用湿润的淀粉碘化钾试纸,能使湿润的淀粉碘化钾试纸变蓝就是氯气,否则不是.
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,电极周围能变红说明产生氢氧根离子,据此分析.
解答:解:Ⅰ、该燃料电池中,正极上投放的是氧化剂,原电池放电时正极上氧气得电子和氢离子反应生成水,电极反应式为2O2+8H++8e-=4H2O;
负极上投放的是燃料,甲烷失电子和水反应生成二氧化碳和氢离子,电极反应式为CH4+2H4O-8e-=CO2+8H+;
所以电池反应式为:CH4+2O4=CO2+2H2O.
故答案为:正极:2O2+8H++8e-=4H2O;负极:CH4+2H4O-8e-=CO2+8H+;总反应:CH4+2O4=CO2+2H2O.
Ⅱ、(1)①该装置是原电池,较活泼的金属铁作负极,石墨作正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-;
故答案为:负;O2+2H2O+4e-=4OH-.
②该原电池放电时,负极上铁失电子生成亚铁离子,正极上氧气得电子和水反应生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁易被氧化生成氢氧化铁,所以溶液中有红褐色沉淀生成.
故答案为:溶液中有红褐色沉淀生成.
③发生的反应方程式为:2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
故答案为:2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(2)①该装置是电解池,E是阴极,F是阳极,阳极上氯离子放电生成氯气,电极反应式为:2Cl--2e-=Cl2↑.
故答案为:阴; 2Cl--2e-=Cl2↑.
②阳极上生成氯气,检验氯气用湿润的淀粉碘化钾试纸,如果用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气.
故答案为:用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气.
(3)若往U型管中滴加酚酞,进行(1)操作时,该装置是原电池,正极上氧气得电子和水反应生成氢氧根离子,导致A附近溶液呈碱性,所以酚酞试液变红.
若往U型管中滴加酚酞,进行(2)操作时,阴极上氢离子放电导致溶液中氢氧根浓度大于氢离子浓度而使溶液呈碱性,加入酚酞试液会变红.
故答案为:A、E
负极上投放的是燃料,甲烷失电子和水反应生成二氧化碳和氢离子,电极反应式为CH4+2H4O-8e-=CO2+8H+;
所以电池反应式为:CH4+2O4=CO2+2H2O.
故答案为:正极:2O2+8H++8e-=4H2O;负极:CH4+2H4O-8e-=CO2+8H+;总反应:CH4+2O4=CO2+2H2O.
Ⅱ、(1)①该装置是原电池,较活泼的金属铁作负极,石墨作正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-;
故答案为:负;O2+2H2O+4e-=4OH-.
②该原电池放电时,负极上铁失电子生成亚铁离子,正极上氧气得电子和水反应生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁易被氧化生成氢氧化铁,所以溶液中有红褐色沉淀生成.
故答案为:溶液中有红褐色沉淀生成.
③发生的反应方程式为:2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
故答案为:2Fe+O2+2H2O=2Fe(OH)2;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(2)①该装置是电解池,E是阴极,F是阳极,阳极上氯离子放电生成氯气,电极反应式为:2Cl--2e-=Cl2↑.
故答案为:阴; 2Cl--2e-=Cl2↑.
②阳极上生成氯气,检验氯气用湿润的淀粉碘化钾试纸,如果用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气.
故答案为:用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气.
(3)若往U型管中滴加酚酞,进行(1)操作时,该装置是原电池,正极上氧气得电子和水反应生成氢氧根离子,导致A附近溶液呈碱性,所以酚酞试液变红.
若往U型管中滴加酚酞,进行(2)操作时,阴极上氢离子放电导致溶液中氢氧根浓度大于氢离子浓度而使溶液呈碱性,加入酚酞试液会变红.
故答案为:A、E
| 周围变红的电极代号(填字母) | 原因 |
| A | O2+2H2O+4e-=4OH-,产生OH- |
| E | 2H++2e-=H2↑ H+反应,促进了水的电离,溶液中c(OH-)>c(H+) |
点评:本题考查了原电池原理和电解池原理,明确原电池和电解池电极上发生反应的类型即可分析解答本题,难度不大,注意电极反应式的书写与电解质溶液的酸碱性有关.

练习册系列答案
相关题目
由周期表中前20号元素组成的单质X2、Y和化合物Z的有关信息如下表,X2、Y 和Z之间的转化关系如右图(其他无关物质已略去)。请回答下列问题:
| 元素X | 易形成-1价18电子的单核离子 |
| 元素Y | 第3周期第ⅥA族 |
| 化合物Z | 所含阳离子有3个电子层 |
| 常温下0.1 mol·L-1的水溶液pH=13 |
(1)用化学方程式表示X2在工业生产上的一种用途 。
(2) 比较元素X与Y的氢化物稳定性: 比 稳定(填氢化物化学式)。
(3)将0.24 mol Y氧化物YO2和 0.11 mol氧气放入容积为1 L的密闭容器中,一定条件下反应达到平衡,得到0.12 mol YO3气体,同时放出热量11.8kJ。
①该反应平衡常数= 。
②该反应的热化学方程式为 。
(4) C能与稀硫酸反应生成能使品红溶液褪色的气体,D中所含阴、阳离子的电子层排布相同。
①写出Y与Z反应的离子方程式
②将20 mL 0.5 mol·L-1 C溶液逐滴加入到V mL 0.2 mol·L-1 KMnO4溶液(硫酸酸化)中,溶液恰好褪色(此时Mn元素恰好变为Mn2+)。计算V= 。
(5)用石墨作电极,在隔膜电解槽中电解A的溶液,可制得Z的水溶液,请写出甲烷燃料电池(Z的水溶液为电解质溶液)负极的电极反应式

 英国国家海洋学中心于2009年8月14日发布新闻公报说,中心的研究人员及其同行利用声呐等手段探测到北极海洋中存在大量甲烷气泡,证实了全球变暖会使海底释放大量甲烷的说法。研究人员认为,这些甲烷可能会反过来加剧全球变暖。
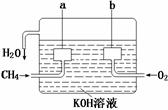
英国国家海洋学中心于2009年8月14日发布新闻公报说,中心的研究人员及其同行利用声呐等手段探测到北极海洋中存在大量甲烷气泡,证实了全球变暖会使海底释放大量甲烷的说法。研究人员认为,这些甲烷可能会反过来加剧全球变暖。 (2)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的电池,氢气虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如甲烷(天然气)、汽油等。电池的构造如图所示:两个电极均由多孔碳制成,通入的气体由孔隙中流出,并从电极表面放出。
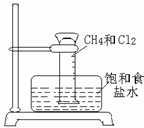
(2)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的电池,氢气虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如甲烷(天然气)、汽油等。电池的构造如图所示:两个电极均由多孔碳制成,通入的气体由孔隙中流出,并从电极表面放出。 (3)某课外活动小组利用右图所示装置探究甲烷于氯气的反应。根据题意,回答下列问题:
(3)某课外活动小组利用右图所示装置探究甲烷于氯气的反应。根据题意,回答下列问题: