摘要: (1) B 接 J . I 接 K . A 接 C . D 接 G . H 接 E . (2)装置Ⅵ的作用是 干燥与除杂 ,装置Ⅳ的作用是 吸水 . (3)冷凝管理冷却水的流向是从 Q 进入.从 F 流出. (4)实验时应先点燃 Ⅰ 处酒精灯.加热温度应大于 231 ℃.待 熔化 即可停止加热. (5)已知四氯化锡遇水强烈水解.产物之一是固态二氧化锡.那么四氯化锡水解的化学方程式为 略 . 6)如果将制取的四氯化锡少许暴露于空气中.预期可看到的现象是 白雾 . (7)为了防止污染空气.在装置的最后应 NaOH溶液吸收 .
网址:http://m.1010jiajiao.com/timu3_id_346452[举报]
(2010?杭州二模)现有一定量含有NaOH杂质的Na2O2试样5.00g,分成等质量两份,用两种方法测定Na2O2试样的纯度.请填写下列空白:
(1)第一种方法:取第一份试样,从图1中选用适当的实验装置,设计一个实验以测定过氧化钠的纯度(可供选用的反应物只有CaCO3固体、MnO2固体、6mol?L-1盐酸和蒸馏水).
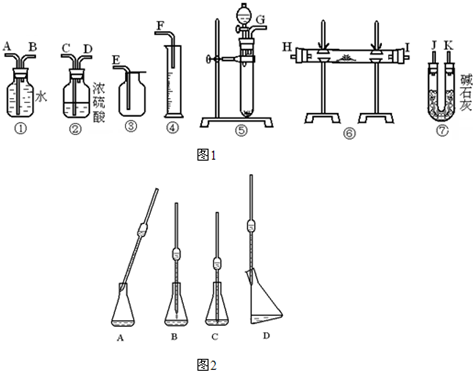
①若实验要求装置尽可能简单,应选用图1中的装置是(只要求写出图中装置的标号)
②所选用装置的连接顺序应是(填各接口的字母;连接胶管略).
③若实验过程中共产生氧气140mL(已折算成标准状况),则试样中过氧化钠的纯度为
(2)第二种方法:取第二份试样,配成250.00mL溶液,用0.255 0mol?L-1的标准盐酸滴定.
①取上述所配溶液25.00mL于锥形瓶中,操作如图2所示(手持部分省略):正确的操作是图
②滴定操作平行实验的数据记录如下表:
由表中数据计算样品中Na2O2纯度为
(3)若上述两个实验中不存在重大的操作失误,测得的实验数据也是真实可靠的,但以上两种方法测得的Na2O2纯度数据误差较大.
①你认为上述两种方法中,哪种方法更为可靠
②产生较大实验误差的原因最可能是
③在题中所给出的仪器和药品范围内,如何用简单的方法加以改进,使实验误差大为减少,写出改进的方法
查看习题详情和答案>>
(1)第一种方法:取第一份试样,从图1中选用适当的实验装置,设计一个实验以测定过氧化钠的纯度(可供选用的反应物只有CaCO3固体、MnO2固体、6mol?L-1盐酸和蒸馏水).

①若实验要求装置尽可能简单,应选用图1中的装置是(只要求写出图中装置的标号)
⑤①④
⑤①④
.②所选用装置的连接顺序应是(填各接口的字母;连接胶管略).
(G)接(A)(B)接(F)
(G)接(A)(B)接(F)
.③若实验过程中共产生氧气140mL(已折算成标准状况),则试样中过氧化钠的纯度为
39%
39%
.(2)第二种方法:取第二份试样,配成250.00mL溶液,用0.255 0mol?L-1的标准盐酸滴定.
①取上述所配溶液25.00mL于锥形瓶中,操作如图2所示(手持部分省略):正确的操作是图
D
D
,取溶液所用仪器的名称是移液管
移液管
.②滴定操作平行实验的数据记录如下表:
| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
78%
78%
.(3)若上述两个实验中不存在重大的操作失误,测得的实验数据也是真实可靠的,但以上两种方法测得的Na2O2纯度数据误差较大.
①你认为上述两种方法中,哪种方法更为可靠
第二种方法
第二种方法
?②产生较大实验误差的原因最可能是
过氧化钠和水反应一部分生成过氧化氢,使氧气不能全部逸出
过氧化钠和水反应一部分生成过氧化氢,使氧气不能全部逸出
.③在题中所给出的仪器和药品范围内,如何用简单的方法加以改进,使实验误差大为减少,写出改进的方法
反应前向过氧化钠中加入少量二氧化锰固体
反应前向过氧化钠中加入少量二氧化锰固体
.现有一定量含有Na2O杂质的Na2O2试样.请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体,6摩尔/升盐酸和蒸馏水).
请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式.
(2)应选用的装置是(只要求写出图中装置的标号)
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略).
查看习题详情和答案>>
请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式.
2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH
2Na2O2+2H2O=4NaOH+O2↑;Na2O+H2O=2NaOH

(2)应选用的装置是(只要求写出图中装置的标号)
⑤②①④
⑤②①④
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略).
(G)接(D)(C)(A)(B)接(F)
(G)接(D)(C)(A)(B)接(F)
.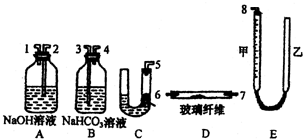 (实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低.
(实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低.实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水试回答:(1)上述装置的连接顺序是(填各接口的编号,其中连接胶管及夹持装置均省略):
53467218(6、7可颠倒)
53467218(6、7可颠倒)
.(2)装置C中放入的反应物是
大理石
大理石
和盐酸
盐酸
.(3)装置A的作用是
吸收氧气中未反应的二氧化碳
吸收氧气中未反应的二氧化碳
,装置B的作用是吸收中混有的HCl
吸收中混有的HCl
.(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意
a
a
和c
c
(填写字母编号).a.视线与凹液面最低数相平b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平d.读数时不一定使甲、乙管液面相平.
 现有含CaO杂质的CaC2试样.某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度.请填写下列空白:
现有含CaO杂质的CaC2试样.某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度.请填写下列空白:(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度.所选用装置的连接顺序应是(填各接口的字母):
E、C、D、B
E、C、D、B
.| 读数次数 | 质量/g | |
| 锥形瓶+水+试样 | 第1次 | 196.30 |
| 第2次 | 196.15 | |
| 第3次 | 196.05 | |
| 第4次 | 196.00 | |
| 第5次 | 196.00 |
计算CaC2的质量分数时,必需用的数据是
试样质量、锥形瓶和水的质量、第4、5次读数
试样质量、锥形瓶和水的质量、第4、5次读数
.不必作第6次读数的原因是第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全
第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全
.此试样中CaC2的质量分数为82%
82%
.(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:

①操作Ⅱ的名称是
蒸发
蒸发
.②还需直接测定的物理量是
CaCl2质量
CaCl2质量
.③在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果
偏大
偏大
(填“偏大”、“偏小”或“不变”).④请指出该实验方案的2个不足之处
由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大
由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大
⑤请改进这个实验方案,至少解决其中1个不足之处
可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量
可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量
.