题目内容
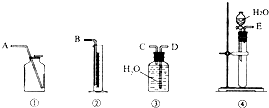 现有含CaO杂质的CaC2试样.某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度.请填写下列空白:
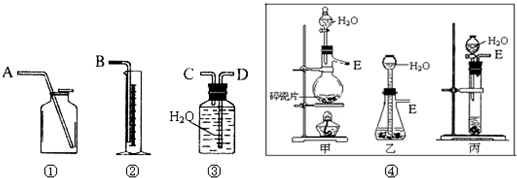
现有含CaO杂质的CaC2试样.某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度.请填写下列空白:(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度.所选用装置的连接顺序应是(填各接口的字母):
E、C、D、B
E、C、D、B
.| 读数次数 | 质量/g | |
| 锥形瓶+水+试样 | 第1次 | 196.30 |
| 第2次 | 196.15 | |
| 第3次 | 196.05 | |
| 第4次 | 196.00 | |
| 第5次 | 196.00 |
计算CaC2的质量分数时,必需用的数据是
试样质量、锥形瓶和水的质量、第4、5次读数
试样质量、锥形瓶和水的质量、第4、5次读数
.不必作第6次读数的原因是第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全
第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全
.此试样中CaC2的质量分数为82%
82%
.(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:
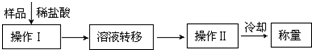
①操作Ⅱ的名称是
蒸发
蒸发
.②还需直接测定的物理量是
CaCl2质量
CaCl2质量
.③在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果
偏大
偏大
(填“偏大”、“偏小”或“不变”).④请指出该实验方案的2个不足之处
由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大
由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大
⑤请改进这个实验方案,至少解决其中1个不足之处
可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量
可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量
.分析:(1)乙炔气体难溶于水可以用排水量气方法测定气体体积;
(2)在锥形瓶中生成乙炔,气体逸出,剩余物质的质量减小,所以根据称量反应前后锥形瓶和物质的质量变化,得到生成气体的质量,根据化学方程式计算乙炔的质量,得到样品的纯度,所以需要称量反应前锥形瓶和水的质量、样品质量、反应后锥形瓶加水加式样的质量;
第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全,说明反应在第四次读数时已经结束;
锥形瓶中发生反应CaC2+2H2O→Ca(OH)2+C2H2↑,锥形瓶+水+试样总质量减少为生成C2H2的质量,根据方程式计算样品中CaC2的质量,进而计算CaC2的质量分数.
(3)①根据反应过程和生成产物的性质分析判断,通过蒸发溶液得到固体,进行质量称量;
②加入盐酸反应后生成氯化钙溶液,实验目的是最后称量氯化钙的质量,应将溶液蒸发,并放在干燥器中冷却后称量固体质量;
③在转移溶液时,如溶液转移不完全,会导致测定的氯化钙的质量偏小,令原样品中的氧化钙物质的量为X,碳化钙物质的量为Y,未损耗时称量的氯化钙质量为Z,则得到:56X+64Y=1.6;X+Y=Z/111;整理判断.
④由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大
⑤由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量,将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量.
(2)在锥形瓶中生成乙炔,气体逸出,剩余物质的质量减小,所以根据称量反应前后锥形瓶和物质的质量变化,得到生成气体的质量,根据化学方程式计算乙炔的质量,得到样品的纯度,所以需要称量反应前锥形瓶和水的质量、样品质量、反应后锥形瓶加水加式样的质量;
第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全,说明反应在第四次读数时已经结束;
锥形瓶中发生反应CaC2+2H2O→Ca(OH)2+C2H2↑,锥形瓶+水+试样总质量减少为生成C2H2的质量,根据方程式计算样品中CaC2的质量,进而计算CaC2的质量分数.
(3)①根据反应过程和生成产物的性质分析判断,通过蒸发溶液得到固体,进行质量称量;
②加入盐酸反应后生成氯化钙溶液,实验目的是最后称量氯化钙的质量,应将溶液蒸发,并放在干燥器中冷却后称量固体质量;
③在转移溶液时,如溶液转移不完全,会导致测定的氯化钙的质量偏小,令原样品中的氧化钙物质的量为X,碳化钙物质的量为Y,未损耗时称量的氯化钙质量为Z,则得到:56X+64Y=1.6;X+Y=Z/111;整理判断.
④由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大
⑤由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量,将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量.
解答:解:(1)乙炔气体难溶于水可以用排水量气方法测定气体体积,装置的连接顺序是E、C、D、B;
故答案为:装置的连接顺序是E、C、D、B.
(2)在锥形瓶中生成乙炔,气体逸出,剩余物质的质量减小,所以根据称量反应前后锥形瓶和物质的质量变化,得到生成气体的质量,根据化学方程式计算乙炔的质量,得到样品的纯度,所以需要称量反应前锥形瓶和水的质量、样品质量、反应后锥形瓶加水加式样的质量,第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全,说明反应在第四次读数时已经结束,
锥形瓶中发生反应CaC2+2H2O→Ca(OH)2+C2H2↑,生成C2H2的质量为(195+1.5)g-196g=0.5g,令CaC2质量为m,则:
CaC2+2H2O→Ca(OH)2+C2H2↑
64g 26g
m 0.5g
所以m=
=
g,CaC2的质量分数为
×100%=82%.
故答案为:试样质量、锥形瓶和水的质量、第4、5次读数;第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全;82%
(3)①加入盐酸反应后生成氯化钙溶液,实验目的是最后称量氯化钙的质量,应将溶液蒸发,所用仪器为蒸发皿,并用玻璃棒搅拌,加热后所得固体放在干燥器中冷却后称量;
故答案为:蒸发;
②加入盐酸反应后生成氯化钙溶液,实验目的是最后称量氯化钙的质量,需要直接测定CaCl2质量;
故答案为:CaCl2质量.
③在转移溶液时,如溶液转移不完全,会导致测定的氯化钙的质量偏小,令原样品中的氧化钙物质的量为X,碳化钙物质的量为Y,未损耗时称量的氯化钙质量为Z,则得到:56X+64Y=1.6;X+Y=Z/111,整理的Y=0.2-
,所以称量的氯化钙损耗越多,计算得到的碳化钙的质量越大,所占质量分数越大,在转移溶液时,如溶液转移不完全,损耗氯化钙,Z减少,Y增大,CaC2质量分数增大,所以测量结果偏大;
故答案为:偏大.
④该实验方案的不足之处:由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大.
故答案为:由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大.
⑤由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量,可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量.
故答案为:可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量.
故答案为:装置的连接顺序是E、C、D、B.
(2)在锥形瓶中生成乙炔,气体逸出,剩余物质的质量减小,所以根据称量反应前后锥形瓶和物质的质量变化,得到生成气体的质量,根据化学方程式计算乙炔的质量,得到样品的纯度,所以需要称量反应前锥形瓶和水的质量、样品质量、反应后锥形瓶加水加式样的质量,第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全,说明反应在第四次读数时已经结束,
锥形瓶中发生反应CaC2+2H2O→Ca(OH)2+C2H2↑,生成C2H2的质量为(195+1.5)g-196g=0.5g,令CaC2质量为m,则:
CaC2+2H2O→Ca(OH)2+C2H2↑
64g 26g
m 0.5g
所以m=
| 64g×0.5g |
| 26g |
| 16 |
| 13 |
| ||
| 1.5g |
故答案为:试样质量、锥形瓶和水的质量、第4、5次读数;第4、5次实验读数相同,表明锥形瓶内质量已达恒重,反应进行完全;82%
(3)①加入盐酸反应后生成氯化钙溶液,实验目的是最后称量氯化钙的质量,应将溶液蒸发,所用仪器为蒸发皿,并用玻璃棒搅拌,加热后所得固体放在干燥器中冷却后称量;
故答案为:蒸发;
②加入盐酸反应后生成氯化钙溶液,实验目的是最后称量氯化钙的质量,需要直接测定CaCl2质量;
故答案为:CaCl2质量.
③在转移溶液时,如溶液转移不完全,会导致测定的氯化钙的质量偏小,令原样品中的氧化钙物质的量为X,碳化钙物质的量为Y,未损耗时称量的氯化钙质量为Z,则得到:56X+64Y=1.6;X+Y=Z/111,整理的Y=0.2-
| 7Z |
| 111 |
故答案为:偏大.
④该实验方案的不足之处:由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大.
故答案为:由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量;CaO和CaC2的摩尔质量接近,实验误差会很大.
⑤由于CaCl2具有很强的吸水性,称量的不一定是无水CaCl2的质量,可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量.
故答案为:可以将Ca2+转化为CaCO3或CaC2O4沉淀,过滤后称其质量.
点评:本题考查学生对的实验方案原理的理解与评价、物质组成含量的测定、化学计算等,题目难度较大,理清实验原理是关键,是对学生综合能力想考查,需要学生具备扎实的基础知识.

练习册系列答案
相关题目