摘要:16] A
网址:http://m.1010jiajiao.com/timu3_id_345524[举报]
A、B、C、D、E、F属于短周期主族元素.A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零,C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差.
(1)离子B-的结构示意图为
 ;化合物CE2的分子属于
;化合物CE2的分子属于
 .
.
(2)A、E、F形成的简单离子的半径由大到小的顺序为
(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W?8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一.有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3.该电池的负极反应式为
查看习题详情和答案>>
(1)离子B-的结构示意图为


非极性
非极性
分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程

(2)A、E、F形成的简单离子的半径由大到小的顺序为
S2->O2->Na+
S2->O2->Na+
(用离子符号表示);元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)金刚石(石墨)>晶体硅>氧气
金刚石(石墨)>晶体硅>氧气
.(3)由B、C可以构成的最简单的化合物W,取16.0g分子式为W?8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
.(4)使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一.有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3.该电池的负极反应式为
C4H10+13O2--26e-=4CO2+5H2O
C4H10+13O2--26e-=4CO2+5H2O
,电池工作时,电解质里的CO32-向负
负
极移动.A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
(1)在标准状况下为液体的卤素单质是
(2)A的相对分子质量为
(3)写出B与水反应的化学方程式
(4)卤素单质B、C、D的氧化性由大到小的顺序为
查看习题详情和答案>>
| 卤素单质 | 密度(标准状况下) | 沸点/℃ | 熔点/℃ | 溶解度(标准状况下,100g水中) |
| A | 1.696 g?l-1 | -188.1 | -219.6 | -- |
| B | 3.214 g?l-1 | -34.6 | -101 | 226 cm3 |
| C | 3.119 g?cm-3 | 58.78 | -7.2 | 4.16 g |
| D | 4.93 g?cm-3 | 184.4 | 113.5 | 0.029 g |
C
C
(填字母,下同),为固体的卤素单质是D
D
.(2)A的相对分子质量为
38
38
(保留整数)(3)写出B与水反应的化学方程式
Cl2+H2O═HCl+HClO
Cl2+H2O═HCl+HClO
(4)卤素单质B、C、D的氧化性由大到小的顺序为
Cl2>Br2>I2
Cl2>Br2>I2
(用化学式表示) A、B、C、D、E五种物质(或离子)均含有同一种短周期元素,它们之间有如转化关系:
A、B、C、D、E五种物质(或离子)均含有同一种短周期元素,它们之间有如转化关系:(1)若A为非金属单质,C、D的相对分子质量相差16.0.1mol/L E溶液中只有3种离子,且常温下溶液中的pH=1.A→C的反应中,每转移1mol e-就会吸热45kJ,写出该反应的热化学方程式:
N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol
N2(g)+O2(g)=2NO(g)△H=+180 kJ/mol
.(2)若A为金属单质,B、C均属于盐类,D是一种白色沉淀.若B的水溶液呈酸性,C的水溶液呈碱性.写出C→D反应的离子方程式:
AlO2-+H++H2O=Al(OH)3↓
AlO2-+H++H2O=Al(OH)3↓
;写出金属A的电子排布式:1s22s22p63s23p1
1s22s22p63s23p1
.(3)若A-E均为化合物.A是淡黄色固体;B、C、E三种溶液在物质的量浓度相等时,B溶液的pH最大,E溶液的pH最小.
请书写C溶液中的物料守恒式:
| 1 |
| 2 |
| 1 |
| 2 |
c(H+)=c(OH-)+2c(H2CO3)+c(HCO3-)
c(H+)=c(OH-)+2c(H2CO3)+c(HCO3-)
.A、B、C、D、E、F均为短周期元素,其原子序数依次增大.已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素.根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为
(4)C2A4─空气燃料电池是一种碱性燃料电池.电解质溶液是20%~30%的KOH溶液.则燃料电池放电时:正极的电极反应式是
(5)已知:2CD2(g)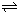 C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
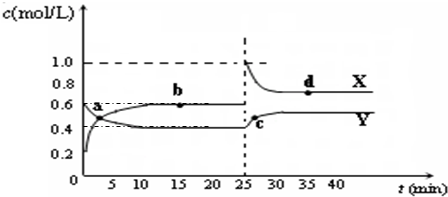
①a、b、c、d四个点中,化学反应处于平衡状态的是
②25min时,增加了
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
查看习题详情和答案>>
(1)B与D形成化合物BD2的结构式为
O═C═O
O═C═O
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
.
| ||
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为
H++HSO3-═SO2↑+H2O
H++HSO3-═SO2↑+H2O
;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)CO32-+H2O HCO3-+OH-
HCO3-+OH-
 HCO3-+OH-
HCO3-+OH-CO32-+H2O HCO3-+OH-
HCO3-+OH-
. HCO3-+OH-
HCO3-+OH-(4)C2A4─空气燃料电池是一种碱性燃料电池.电解质溶液是20%~30%的KOH溶液.则燃料电池放电时:正极的电极反应式是
O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
.(5)已知:2CD2(g)
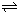 C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
①a、b、c、d四个点中,化学反应处于平衡状态的是
bd
bd
点.②25min时,增加了
NO2
NO2
(填物质的化学式)0.8
0.8
mol.③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
cdba
cdba
(填字母).A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
请回答下列问题:
(1)A元素在周期表中的位置为
(2)A、D的氢化物相互反应,产生白色固体,写出该反应的化学方程式
(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是

查看习题详情和答案>>
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中,与D形成的化合物是生活中最常用的调味品 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A元素在周期表中的位置为
第二周期,ⅤA族
第二周期,ⅤA族
;其氢化物水溶液能使酚酞变红的原因用电离方程式解释为NH3?H2O?NH4++OH-
NH3?H2O?NH4++OH-
.(2)A、D的氢化物相互反应,产生白色固体,写出该反应的化学方程式
NH3+HCl═NH4Cl
NH3+HCl═NH4Cl
.(3)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为
离子键和共价键
离子键和共价键
.(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①③
①③
.①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)若在D与E组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极出现的现象是
黄色溶液慢慢变为浅绿色
黄色溶液慢慢变为浅绿色
,负极的反应式为Cu-2e-=Cu2+
Cu-2e-=Cu2+
.