摘要: 下列各表达式.错误的是 ① 氯化钠水解:NaCL = OH+ H ② 铜在硫蒸气中燃烧:2Cu + S =Cu2S ③ 钢铁吸氧腐蚀时正极的反应:2H2O + O2 + 4e = 4OH ④ 氢气燃烧的热化学方程式:H2(气) + (气) = H2O + 285千焦 ①.④ ③.④
网址:http://m.1010jiajiao.com/timu3_id_34488[举报]
下列各排列顺序错误的是( )
A. 酸性:HclO4>H2SO4>HaPO4>HSiO4
B. 碱性:RbOH>Ca(OH)2>Mg(OH)2>Al(OH)3
C. 热稳定性:H2S>H2O>PH3>AsH3
D. 原子半径:Na>S>O>F
查看习题详情和答案>>
下列各排列顺序错误的是( )
A. 酸性:HclO4>H2SO4>HaPO4>HSiO4
B. 碱性:RbOH>Ca(OH)2>Mg(OH)2>Al(OH)3
C. 热稳定性:H2S>H2O>PH3>AsH3
D. 原子半径:Na>S>O>F
查看习题详情和答案>>
工业制硝酸的主要反应是4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ/mol(a>0)
(1)如图将4molNH3和5molO2放入容器中,达到平衡时,放出热量0.8a kJ,则反应时转移的电子数为 mol.
(2)若其他条件不变,下列关系图中错误的是 (选填序号)
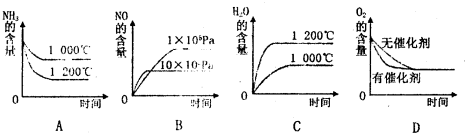
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表
①反应在第2min到第4min时,反应速率v(O2)= .
②第2min时改变了条件,改变的条件可能是 .
A.升高温度B.使用了催化剂C.减小压强D.增加了生成物
③在相同的温度下,起始向容器中加入NH、O2、NO和H2O(g)的浓度都为1mol/L,则该反应将向 方向进行(填“正反应”、“逆反应”、“不移动”).
(4)工业上用水吸收二氧化氮生产硝酸,生成的气体经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其他损失),现有一定量的NO2经过 次循环操作后,才能使95%以上的NO2转化为HNO3.
(5)成品硝酸的浓度为60%~70%,为了制浓硝酸,常用Mg(NO3)2作吸水剂,然后进行蒸馏,不用CaCl或MgCl2作吸水剂的原因是 .
查看习题详情和答案>>
(1)如图将4molNH3和5molO2放入容器中,达到平衡时,放出热量0.8a kJ,则反应时转移的电子数为
(2)若其他条件不变,下列关系图中错误的是

(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表
| 浓度 时间 |
c(NH3) | c(O2) | c(NO) | c(H2O) |
| 起始 | 4.0 | 5.4 | 0 | 0 |
| 第2min | 3.2 | 1 | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
②第2min时改变了条件,改变的条件可能是
A.升高温度B.使用了催化剂C.减小压强D.增加了生成物
③在相同的温度下,起始向容器中加入NH、O2、NO和H2O(g)的浓度都为1mol/L,则该反应将向
(4)工业上用水吸收二氧化氮生产硝酸,生成的气体经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其他损失),现有一定量的NO2经过
(5)成品硝酸的浓度为60%~70%,为了制浓硝酸,常用Mg(NO3)2作吸水剂,然后进行蒸馏,不用CaCl或MgCl2作吸水剂的原因是
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去).试回答:

(1)若A是乙醇,则C的结构简式是
A.乙醇汽油是一种新型的化合物
B.汽车使用乙醇汽油能减少有害气体的排放
C.工业常用裂化的方法提高汽油的产量
D.用玉米、高粱发酵可以制得乙醇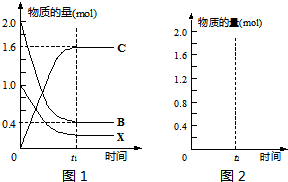
(2)若A是一种工业制硫酸的含金属元素矿物质主要成分,则A的化学式为
①物质B的转化率
②求该温度下反应②的平衡常数
③在上述相同条件下,向相同的容器中投入2mol C,t2时刻达到平衡.请在图2中画出从反应开始至平衡后各物质物质的量与时间的关系图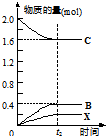
 .
.
查看习题详情和答案>>

(1)若A是乙醇,则C的结构简式是
CH3COOH
CH3COOH
,反应①的化学方程式2CH3CH2OH+O2
2CH3CHO+2H2O
| ||
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
;2001年5月,中国宣布将推广“车用乙醇汽油”,所谓乙醇汽油就是在无铅汽油里加入适量乙醇混合而成的一种燃料.下列叙述中一定错误的是
| ||
| △ |
A
A
.A.乙醇汽油是一种新型的化合物
B.汽车使用乙醇汽油能减少有害气体的排放
C.工业常用裂化的方法提高汽油的产量
D.用玉米、高粱发酵可以制得乙醇

(2)若A是一种工业制硫酸的含金属元素矿物质主要成分,则A的化学式为
FeS2
FeS2
,反应②的化学方程式2SO2+O2
2SO3
| 催化剂 |
| △ |
2SO2+O2
2SO3
.某温度T时,在一定条件的2L密闭容器中,反应②从起始到平衡后的关系如图1所示.请据图回答下列问题:| 催化剂 |
| △ |
①物质B的转化率
80%
80%
.②求该温度下反应②的平衡常数
160
160
.③在上述相同条件下,向相同的容器中投入2mol C,t2时刻达到平衡.请在图2中画出从反应开始至平衡后各物质物质的量与时间的关系图