摘要:15.已知把SO2气体通入BaCl2溶液中无沉淀生成.现把下列物质加入或通入溶液中.能出现沉淀的是⑴N2⑵NO2⑶Cl2⑷H2O2⑸H2S⑹NH3⑺SO3⑻KMnO4⑼HCl⑽Na2O2⑾CO2⑿AgNO3 A. 只有⑴⑵⑶⑸⑺⑼ B.只有⑵⑶⑷⑸⑹⑺⑻⑽⑿ C. 只有⑵⑸⑺⑼⑽⑾ D.只有⑵⑶⑸⑺⑼⑾
网址:http://m.1010jiajiao.com/timu3_id_344622[举报]
|
已知2FeSO4 | |
A. |
产生BaSO4和BaSO3两种沉淀 |
B. |
产生BaSO4沉淀,SO2从溶液中逸出 |
C. |
产生BaSO4沉淀,无SO2气体逸出 |
D. |
产生沉淀含BaSO4,并有HCl气体逸出 |
|
已知2FeSO4 | |
| [ ] | |
A. |
产生BaSO4和BaSO3两种沉淀 |
B. |
产生BaSO4沉淀,SO2从溶液中逸出 |
C. |
产生BaSO4沉淀,无SO2气体逸出 |
D. |
产生沉淀含BaSO4,并有HCl气体逸出 |
某非金属单质A经如 A
B
C
D 所示的过程转化为含氧酸D,已知D为强酸,请回答:
(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体.
①写出A的原子结构示意图:

②把B通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀化学式为:
③D的浓溶液在加热的条件下可与Cu反应,该反应的化学方程式为:
(2)若A在常温下为气体,C是红棕色气体.
①写出A单质的电子式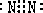
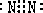 .
.
②C→D的反应中氧化剂与还原剂物质的量之比为:
③写出A与H2反应产物的结构式:
 .
.
查看习题详情和答案>>
| O2 |
| O2 |
| H2O |
(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体.
①写出A的原子结构示意图:


②把B通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀化学式为:
BaSO4
BaSO4
③D的浓溶液在加热的条件下可与Cu反应,该反应的化学方程式为:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
(2)若A在常温下为气体,C是红棕色气体.
①写出A单质的电子式
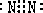
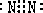
②C→D的反应中氧化剂与还原剂物质的量之比为:
1:2
1:2
③写出A与H2反应产物的结构式:


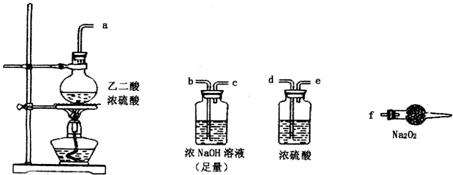
 有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:(1)第一小组同学设计如图装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,则反应的化学方程式为
2Na2O2+2SO2=2Na2SO3+O2
2Na2O2+2SO2=2Na2SO3+O2
.乙同学认为Na2O:与SO2反应除了生成Na2SO3和O2外,还有Na2SO.生成.为检验是否有Na2SO4生成,该同学设计了如下方案:
你认为乙同学的方案是否合理
否
否
(答“是”或“否”);请简要说明两点理由:①
稀HNO3可以把BaSO3氧化为BaSO4
稀HNO3可以把BaSO3氧化为BaSO4
②若反应后的固体有Na2O2残留,溶于水后可把SO32- 氧化为 SO42-
若反应后的固体有Na2O2残留,溶于水后可把SO32- 氧化为 SO42-
.(2)第二小组同学利用下图中的有关装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应.已知:H2C204
| ||
| △ |
Na2CO3
Na2CO3
;验证该产物可选择的试剂是稀H2SO4(或稀HC1)和澄清石灰水
稀H2SO4(或稀HC1)和澄清石灰水
.上述实验中选择的最简单的装置接口连接顺序为abcf
abcf
.
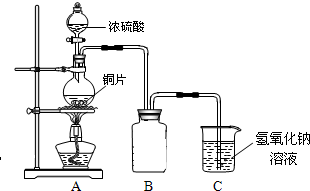 (2011?绵阳模拟)某化学兴趣小组为探究
(2011?绵阳模拟)某化学兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置先进行了有关实验:
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整.
(2)实验中他们取6.4g铜片和12ml 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①请写铜跟浓硫酸反应的化学方程式:
Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑
| ||
Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑
.
| ||
②为什么有一定量的余酸但未能使用铜片完全溶解,你认为原因是:
随反应进行,硫酸浓度变稀,Cu不与稀H2SO4反应
随反应进行,硫酸浓度变稀,Cu不与稀H2SO4反应
.③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是
AD
AD
(填写字母编号).A、铁粉 B、BaCl2溶液 C、银粉 D、Na2CO3溶液
(3)为定量测定余酸的物质的量浓度,甲、乙两同学进行了如下设计:
①甲学生设计方案是:先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度.他认为测定SO2的量的方法有多种,请问下列实验方案中不可行的是
ABC
ABC
(填写字母编号).A、将装置产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量
B、将装置A产生的气体缓缓通入足量的硫酸酸化的KMnO4溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C、用排水法测定装置A产生气体的体积(已折算成标准状况)
D、用排饱和NaHSO3溶液的方法测出装置A产生气体的体积(已折算成标准状况)
②乙同学设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL于锥形瓶中,用标准氢氧化钠溶液进行滴淀(已知:Cu(OH)2开始沉淀的pH约为5),能否通过测出消耗NaOH溶液的体积来求余酸的物质的量的浓度
否
否
(填“能”或“否”),其理由是含Cu2+的溶液显蓝色,干扰终点判断
含Cu2+的溶液显蓝色,干扰终点判断
. Fe2O3+SO2↑+SO3↑,把产生的气体通入BaCl2溶液中,则
Fe2O3+SO2↑+SO3↑,把产生的气体通入BaCl2溶液中,则