摘要:30.将由amolNaHCO3和bmolNaOH组成的固体混合物放在密闭容器中加热至250℃.经充分反应后.排出气体.冷却后.称量残留固体的质量为x克.试写出 a.b表示的x的表达式. (1)当a≤b时.x= , (2)当a>b时.x= .
网址:http://m.1010jiajiao.com/timu3_id_343963[举报]
(2013?重庆模拟)I.将由Na+、Ba2+、Cu2+、SO42-、Cl-组合形成的三种强电解质溶液,分别装入图1装置中的甲、乙、丙三个烧杯中进行电解,电极均为石墨电极.

接通电源,经过一段时间后,测得乙中c电极质量增加.常温下各烧杯中溶液pH与电解时间t的关系如图2(忽略因气体溶解带来的影响).据此回答下列问题:
(1)写出乙烧杯中发生反应的化学方程式
(2)电极f上发生的电极反应为
(3)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是
II.工业上利用BaSO4制备BaCl2的工艺流程如下:

某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验.
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S.Na2S水溶液显碱性的原因是
(2)已知有关反应的热化学方程式如下:
BaSO4(s)+4C(s)
4CO(g)+BaS(s)△H1=+571.2kJ/mol
C(s)+CO2(g)
2CO(g)△H2=+172.5kJ/mol
则反应BaSO4(s)+2C(s)
2CO2(g)+BaS(s)△H3=
(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是
查看习题详情和答案>>

接通电源,经过一段时间后,测得乙中c电极质量增加.常温下各烧杯中溶液pH与电解时间t的关系如图2(忽略因气体溶解带来的影响).据此回答下列问题:
(1)写出乙烧杯中发生反应的化学方程式
2CuSO4+2H2O
2Cu+O2↑+H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+H2SO4
;
| ||
(2)电极f上发生的电极反应为
4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
;(3)若经过一段时间后,测得乙烧杯中c电极质量增加了8g,要使丙烧杯中溶液恢复到原来的状态,应进行的操作是
向丙烧杯中加入水2.25g
向丙烧杯中加入水2.25g
.II.工业上利用BaSO4制备BaCl2的工艺流程如下:

某活动小组的同学在实验室以重晶石(主要成分BaSO4)为原料,对上述工艺流程进行模拟实验.
(1)上述过程中,气体用过量NaOH溶液吸收得到Na2S.Na2S水溶液显碱性的原因是
S2-+H2O?HS-+OH-、HS-+H2O?H2S+OH-
S2-+H2O?HS-+OH-、HS-+H2O?H2S+OH-
(用离子方程式表示).(2)已知有关反应的热化学方程式如下:
BaSO4(s)+4C(s)
| 高温 |
C(s)+CO2(g)
| 高温 |
则反应BaSO4(s)+2C(s)
| 高温 |
+226.2
+226.2
kJ/mol(3)在高温焙烧重晶石过程中必须加入过量的炭,同时还要通入空气,其目的是
使BaSO4得到充分的还原(或提高BaS的产量)
使BaSO4得到充分的还原(或提高BaS的产量)
,硫酸钡和碳反应为吸热反应,炭和氧气反应放热维持反应所需高温
硫酸钡和碳反应为吸热反应,炭和氧气反应放热维持反应所需高温
.(2011?济南一模)A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;
D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4倍;C与E同主族.
请回答下列问题:
(1)X的化学式为
 .
.
(2)元素的非金属性C
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强.
已知(ⅰ) 浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC.
(ⅱ) NaOH溶液与BC2反应的化学方程式为:2NaOH+2BC2═NaBC2+NaBC+H2O NaOH溶液与B、C气体不反应
a.装置①、②、③中盛放的药品依次是
b.通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是
c.能够说明实验已成功的现象是
查看习题详情和答案>>
D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4倍;C与E同主族.
请回答下列问题:
(1)X的化学式为
NH4NO3
NH4NO3
,D的原子结构示意图为

(2)元素的非金属性C
>
>
E(填“>”、“<”或“=”),下列各项中,能说明这一结论的事实有②③
②③
(填序号).①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强.

已知(ⅰ) 浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC.
(ⅱ) NaOH溶液与BC2反应的化学方程式为:2NaOH+2BC2═NaBC2+NaBC+H2O NaOH溶液与B、C气体不反应
a.装置①、②、③中盛放的药品依次是
H2O
H2O
、稀HNO3
稀HNO3
、浓HNO3
浓HNO3
.b.通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是
CO2
CO2
(填一种气体的化学式).c.能够说明实验已成功的现象是
装置②中液面上方气体仍为无色,装置③中液面上方气体由无色变为红棕色
装置②中液面上方气体仍为无色,装置③中液面上方气体由无色变为红棕色
.将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合物液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )


查看习题详情和答案>>
 A、B、D、E、G为短周期元素,其原子序数依次增大.A元素在周期表中原子半径最小,B元素的最高正化合价和最低负化合价的绝对值相等,E元素的原子最外层电子数是次外层的3倍.E和G可形成离子化合物GE.
A、B、D、E、G为短周期元素,其原子序数依次增大.A元素在周期表中原子半径最小,B元素的最高正化合价和最低负化合价的绝对值相等,E元素的原子最外层电子数是次外层的3倍.E和G可形成离子化合物GE.试回答下列问题:
(1)在点燃的条件下,G的单质与化合物BE2反应的方程式
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(2)用电子式表示GE的形成过程
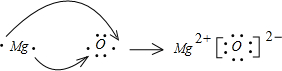
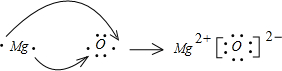
(3)写出在加热条件下B的单质与D的最高价氧化物的水化物的浓溶液反应的化学方程式
C+4HNO3(浓)=CO2↑+4NO2↑+2H2O
C+4HNO3(浓)=CO2↑+4NO2↑+2H2O
.(4)写出由上述元素中的四种元素形成的能溶于水的强电解质的化学式
(NH4)2CO3
(NH4)2CO3
(任写一种).(5)将由A分别与B、D、E组成的化合物按沸点由高到低的顺序写出它们的分子式
H2O、NH3、CH4
H2O、NH3、CH4
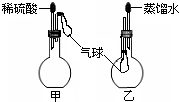
.(6)如图,烧瓶中装有由上述元素形成的化合物.挤压胶头滴管,观察到气球均明显胀大(假定反应完全),则甲烧瓶中盛装的固体化合物的化学式可能为(任写一种)
MgCO3
MgCO3
,乙烧瓶中盛装的气体化合物的化学式可能为(任写一种)NH3
NH3
.