摘要:品红不褪色. Cl2+SO2+2H2O=H2SO4+2HCl
网址:http://m.1010jiajiao.com/timu3_id_343488[举报]
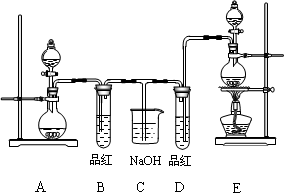
 如图是实验室中制备气体或验证气体性质的装置图.
如图是实验室中制备气体或验证气体性质的装置图.(1)仪器a的名称是
分液漏斗
分液漏斗
.(2)利用上图装置制备纯净、干燥的氯气.
①圆底烧瓶内发生反应的离子方程式为
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
②装置B中的溶液为
饱和NaCl溶液
饱和NaCl溶液
;烧杯中溶液的作用为吸收氯气防污染
吸收氯气防污染
.(3)利用上图装置证明SO2具有漂白性、还原性及生成气体中含有CO2.
圆底烧瓶内加入碳,a中加入浓硫酸,B、D中匀为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水.
①证明SO2具有漂白性的装置是
B
B
,现象是品红褪色
品红褪色
②证明SO2具有还原性的现象是
C中KMnO4溶液褪色
C中KMnO4溶液褪色
③证明生成气体中含有CO2的现象是
D中品红不褪色且石灰水变浑浊
D中品红不褪色且石灰水变浑浊
④D装置的作用是
检验SO2是否除尽
检验SO2是否除尽
.(2010?娄底模拟)钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一.
(1)请写出工业上用电解方法制取钠的化学反应方程式:
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2
CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其他物质.
a.提出合理假设.
假设1:该漂白粉未变质,只含
假设2:该漂白粉全部变质,只含
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3.
b.设计实验方案,进行实验.请在表中写出实验步骤、预期现象和结论
限选的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/L盐酸、品红溶液、新制澄清石灰水.(提示:不必检验Ca2+和Cl-,表格可以不填满)
查看习题详情和答案>>
(1)请写出工业上用电解方法制取钠的化学反应方程式:
2NaCl(熔融)
2Na+Cl2↑
| ||
2NaCl(熔融)
2Na+Cl2↑
.
| ||
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2
|
CaC12、Ca(ClO)2
CaC12、Ca(ClO)2
(填化学式).(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其他物质.
a.提出合理假设.
假设1:该漂白粉未变质,只含
Ca(Cl0)2
Ca(Cl0)2
;假设2:该漂白粉全部变质,只含
CaCO3
CaCO3
;假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3.
b.设计实验方案,进行实验.请在表中写出实验步骤、预期现象和结论
限选的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/L盐酸、品红溶液、新制澄清石灰水.(提示:不必检验Ca2+和Cl-,表格可以不填满)
| 实验步骤 | 预期现象和结论 | |
| ① | 取少量上述漂白粉于试管中, 加入适量的1mol/L盐酸溶解后,将产生的气体通入足量的澄清石灰水中 加入适量的1mol/L盐酸溶解后,将产生的气体通入足量的澄清石灰水中 |
(1)若澄清石灰水未见浑浊,则假设1成立 (2)若澄清石灰水变浑浊,则假设2或3成立 (1)若澄清石灰水未见浑浊,则假设1成立 (2)若澄清石灰水变浑浊,则假设2或3成立 |
| ② | 向步骤①反应后的试管滴入1~2滴品红溶液,振荡 向步骤①反应后的试管滴入1~2滴品红溶液,振荡 |
(1)若品红褪色,固体中存在 Ca(ClO)2,假设3成立;(2)若品红不褪色,则固体中不存在 Ca(ClO)2,假设2成立; (1)若品红褪色,固体中存在 Ca(ClO)2,假设3成立;(2)若品红不褪色,则固体中不存在 Ca(ClO)2,假设2成立; |
| ③ | 此空不填写 此空不填写 |
此空不填写 此空不填写 |
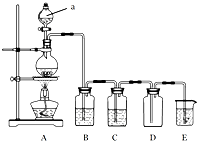
图是实验室中制备气体或验证气体性质的装置图

(1)利用上图装置制备纯净、干燥的氯气.
①圆底烧瓶内发生反应的离子方程式为
②装置B中的溶液为
(2)利用上图装置证明SO2具有漂白性、还原性及生成气体中含有CO2.圆底烧瓶内加入碳,a中加入浓硫酸,B、D中匀为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水.
①证明SO2具有漂白性的装置是
②证明SO2具有还原性的现象是
③证明生成气体中含有CO2的现象是
④D装置的作用是
查看习题详情和答案>>

(1)利用上图装置制备纯净、干燥的氯气.
①圆底烧瓶内发生反应的离子方程式为
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
②装置B中的溶液为
饱和氯化钠溶液
饱和氯化钠溶液
;烧杯中溶液的作用为吸收氯气防止污染空气
吸收氯气防止污染空气
.(2)利用上图装置证明SO2具有漂白性、还原性及生成气体中含有CO2.圆底烧瓶内加入碳,a中加入浓硫酸,B、D中匀为少量品红溶液,C中为足量酸性高锰酸钾溶液,E中为澄清石灰水.
①证明SO2具有漂白性的装置是
B
B
,现象是品红溶液红色褪去
品红溶液红色褪去
;②证明SO2具有还原性的现象是
装置C中高锰酸钾溶液褪色
装置C中高锰酸钾溶液褪色
;③证明生成气体中含有CO2的现象是
D中品红不褪色,装置E中澄清石灰水变浑浊
D中品红不褪色,装置E中澄清石灰水变浑浊
;④D装置的作用是
检验SO2是否除尽
检验SO2是否除尽
.