网址:http://m.1010jiajiao.com/timu3_id_343428[举报]
| ||
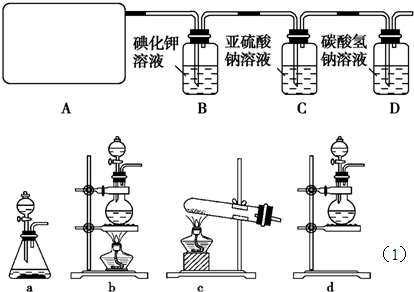
试回答:
(1)该实验中A部分的装置是
(2)B中反应的化学方程式是
(3)写出C中反应的离子方程式
(4)写出在D装置中发生反应的离子方程式
(5)该实验存在明显的缺陷是
(6)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1mol?L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为2Na2S2O3+I2═Na2S4O6+2NaI,反应完成时,共消耗Na2S2O3 200mL.则该漂白粉中Ca(ClO)2的质量分数为
某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4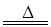 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
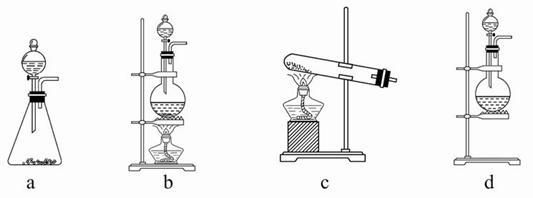
试回答:(1)该实验中A部分的装置是____(填写装置的序号)。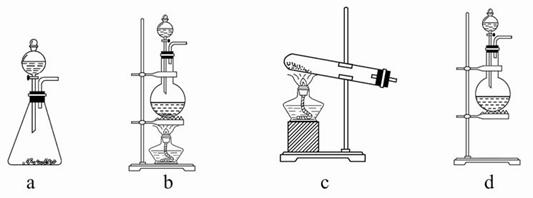
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):____________________________。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式
__________________。
(4)该实验存在明显的缺陷,请你提出改进的方法___________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为: 2Na2S2O3+I2=Na2S4O6 + 2NaI 反应完成时,共用去Na2S2O3
20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为:_____________。
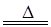 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。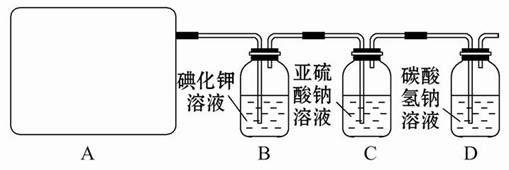
试回答:(1)该实验中A部分的装置是____(填写装置的序号)。
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):____________________________。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式
__________________。
(4)该实验存在明显的缺陷,请你提出改进的方法___________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为: 2Na2S2O3+I2=Na2S4O6 + 2NaI 反应完成时,共用去Na2S2O3
20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为:_____________。

(1)A仪器的名称是
| ||
| ||
(2)漂白粉将在U形管中产生,其化学方程式是
(3)此实验结果所得Ca(ClO)2产率太低.经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应(写出此反应方程式):
(4)漂粉精同盐酸作用产生氯气:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,该反应中每生成1 mol Cl2,转移电子的物质的量为
(16分)氯气可与潮湿的消石灰反应制取少量漂白粉,也可在浓溶液条件下与石灰石反应生成较浓的HClO溶液。
Ⅰ.甲研究性学习小组利用氯气制少量漂白粉(如图所示):
(1)A仪器的名称是 ,所盛试剂是 。
(2)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:
①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是 。此副反应的化学方程式为: 。
②写出另一个副反应的化学方程式 。为避免此副反应发生,可在BC之间加多一个装置,请在答题卷的方框中画出该装置,并标明所用的试剂。
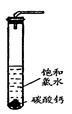
Ⅱ. 乙研究性学习小组研究饱和氯水与石灰石的反应:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。 经检测,上述实验中产生的无色气体均为CO2。请回答:
(3)反应后所得的溶液漂白性增强的原因是 。
(4)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有 。