摘要:原理: 能引起误差的一些操作 误差因素 S/g 试管接触烧杯壁 温度高 偏大 试管内溶剂高出烧杯内的水面 温度低 偏小 温度计插在水浴之中 温度偏低 偏小 溶解时间过短 溶质m小 偏小 溶解过程没有搅拌 溶质m小 偏小 将少量固体倒入蒸发皿内 溶质m大 偏大 晶体未在干燥器内冷却 溶质m大 偏大 仰视温度计刻度 温度偏低 偏大 俯视温度计刻度 温度偏高 偏小 ☆例题精析 [例1] 研究某一化学反应的实验装置如下图所示: A-F属于下列物质中的六种物质:浓硫酸.浓盐酸.浓氨水.稀硫酸.稀盐酸.稀氟水.水.锌粒.铜片.食盐.高锰酸钾.氯化钙.氧化钙.四氧化三铁.氧化铁.氧化铜.氢气.二氧化碳.二氧化氮.一氧化碳.氯气.氯化氢.氨气.氮气.氧气. 实验现象,(1)D物质由黑色变为红色(2)无水硫酸铜粉末放入无色透明的E中得到蓝色溶液(3)点燃的镁条伸入无色无味的F中.镁条表面生成一种灰黄色固体物质.将该发黄色物质放入水中.有气体放出.该气体具有刺激性气味.并能使润湿的红色石蕊试纸变蓝.通过分析回答: l.写出A-F的物质名称: A .B .C .D .E .F .2.写出有关的化学方程式: A与B ,C与D , E与无水硫酸铜 , F与Mg , F与Mg的反应产物与水 . [例2]实验室用NH3还原CuO的方法测定铜的近似相对原子质量.反应的化学方程式为:2NH3+3CuO=N2+3Cu+3H2O .试回答: (1)如果选用测定反应物CuO 和生成物H2O 的质量时.请用下列仪器设计一个简单的实验方案. ①仪器的连接顺序(用字母编号表示.仪器可重复使用) , d中浓硫酸的作用是 . .实验完毕时观察到a 中的现象是 . ②列出计算铜的相对原子质量的表达式 ③下列情况可使测定结果偏大的是: a CuO 未全部被还原为铜 b CuO 受潮 c CuO 中混有Cu (2)如果仍采用上述仪器装置,其它方案可选用测定的物理量有 . A m B m(N2)和m(H2O ) C m(Cu)和m (H2O ) D m(NH3) 和m(CuO) [例3]为测定工业纯碱中的Na2CO3 的质量分数.某学生设计的实验装置如图所示: (1)准确称取盛有碱石灰的干燥管的质量(设为W1) (2)准确称取一定质量的纯碱(设为W0).并放入烧瓶中.从分液漏斗中缓缓滴入稀硫酸.待不再生成气体后.称干燥管的总质量(设为W2).该学生导出的计算公式为: 试回答:(1)W2 - W1表示什么? (2)如果不计称量误差.该生的实验结果有无明显误差?如有.是偏大还是偏小?请简要说明理由并提出补救措施.
网址:http://m.1010jiajiao.com/timu3_id_341129[举报]
NO分子因污染空气而臭名昭著.近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究的热点,NO亦被称为“明星分子”.请回答下列问题.
(1)NO对环境的危害在于
A、破坏臭氧层 B、高温下能使一些金属被氧化 C、造成酸雨 D、与人体血红蛋白结合
(2)在含Cu+(亚铜离子)的酶的活化中心,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式
(3)在常温下,把NO气体压缩到100大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力
就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式
(4)解释变化(3)中为什么最后气体总压力小于原压力大的
?
(5)NO成为“臭名昭著的明星分子”所包含的哲学原理是
查看习题详情和答案>>
(1)NO对环境的危害在于
ACD
ACD
(填以下项目的编号).A、破坏臭氧层 B、高温下能使一些金属被氧化 C、造成酸雨 D、与人体血红蛋白结合
(2)在含Cu+(亚铜离子)的酶的活化中心,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式
Cu++NO2-+2H+=Cu2++NO↑+H2O
Cu++NO2-+2H+=Cu2++NO↑+H2O
.(3)在常温下,把NO气体压缩到100大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力
| 2 |
| 3 |
3NO=N2O+NO2
3NO=N2O+NO2
.(4)解释变化(3)中为什么最后气体总压力小于原压力大的
| 2 |
| 3 |
反应2NO2?N2O4,而使压力略小于原来的
| 2 |
| 3 |
反应2NO2?N2O4,而使压力略小于原来的
.| 2 |
| 3 |
(5)NO成为“臭名昭著的明星分子”所包含的哲学原理是
量变引起质变
量变引起质变
.《化学与生活》
(1)现有下列物质:维生素A、维生素C、碘元素、铁元素、淀粉、油脂.请选择正确答案填在相应的空格里.
①人体缺乏某种维生素会引起夜盲症,这种维生素是
②人体缺乏某种微量元素会发生贫血,这种微量元素是
③既能为人体提供热量,又能提供必需脂肪酸的物质是
(2)了解一些用药常识,有利于自我保健.现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝.
①其中属于解热镇痛的药物是
②青霉素的作用是
③碳酸镁可治疗胃酸过多的原理是
④药片常用淀粉作为黏合剂,淀粉水解的最终产物是
(3)生活中处处有化学,化学已渗透到我们的“衣、食、住、行”之中.
①衣:鉴别真假羊毛衫的方法是先取样,再
②食:水是人类生存的必需物质.在净水过程中,明矾作为
③住:玻璃和钢铁是常用的建筑材料.普通玻璃是由
④行:铝可用于制造交通工具,铝制品不易生锈的原因是
查看习题详情和答案>>
(1)现有下列物质:维生素A、维生素C、碘元素、铁元素、淀粉、油脂.请选择正确答案填在相应的空格里.
①人体缺乏某种维生素会引起夜盲症,这种维生素是
维生素A
维生素A
.②人体缺乏某种微量元素会发生贫血,这种微量元素是
铁元素
铁元素
.③既能为人体提供热量,又能提供必需脂肪酸的物质是
油脂
油脂
.(2)了解一些用药常识,有利于自我保健.现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝.
①其中属于解热镇痛的药物是
阿司匹林
阿司匹林
.②青霉素的作用是
消炎
消炎
.③碳酸镁可治疗胃酸过多的原理是
MgCO3+H+═Mg2++H2O+CO2↑
MgCO3+H+═Mg2++H2O+CO2↑
(用离子方程表示).④药片常用淀粉作为黏合剂,淀粉水解的最终产物是
葡萄糖
葡萄糖
.(3)生活中处处有化学,化学已渗透到我们的“衣、食、住、行”之中.
①衣:鉴别真假羊毛衫的方法是先取样,再
在酒精灯上燃烧,如果有烧焦羽毛的味道,说明是真羊毛衫,否则为假的
在酒精灯上燃烧,如果有烧焦羽毛的味道,说明是真羊毛衫,否则为假的
.②食:水是人类生存的必需物质.在净水过程中,明矾作为
混凝
混凝
剂;氯气或漂白粉作用为杀菌消毒
杀菌消毒
.③住:玻璃和钢铁是常用的建筑材料.普通玻璃是由
Na2SiO3、CaSiO3、SiO2
Na2SiO3、CaSiO3、SiO2
等物质组成的;钢铁制品不仅可发生化学腐蚀,在潮湿的空气中还能发生电化学
电化学
腐蚀.④行:铝可用于制造交通工具,铝制品不易生锈的原因是
表面有一层致密的氧化铝薄膜
表面有一层致密的氧化铝薄膜
_;橡胶是制造轮胎的重要原料,天然橡胶通过硫化
硫化
措施可增大强度和弹性.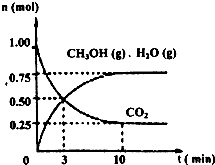 2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验:
某温度下,在容积为2L的密闭容器中,充入1mol CO2和3.25mol H2,在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间变化如右图所示:
①从反应开始到平衡,氢气的平均反应速率v(H2)=
0.1125mol/(L?min)
0.1125mol/(L?min)
.②下列措施中一定不能使n(CH3OH)/n(CO2)增大的是:
D
D
.A.降低温度 B.缩小容器的容积 C.将水蒸气从体系中分离 D.使用更有效的催化剂
(2)常温常压下,饱和CO 2水溶液的pH=5.6,c(H2CO3)=1.5×l0-5mol?L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的电离平衡常数K=
4.2×10-7
4.2×10-7
.(已知:10 -5.6=2.5×l0-6).(3)标准状况下,将1.12LCO2通入100mL 1mol?L-1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为
c(Na+)>c(CO2-3)>c(OH-)>c(HCO-3)>c(H+)
c(Na+)>c(CO2-3)>c(OH-)>c(HCO-3)>c(H+)
;(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示
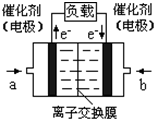 意图,则a处通入的是
意图,则a处通入的是乙醇
乙醇
(填“乙醇”或“氧气”),b处电极上发生的电极反应是:
O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
.(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为
5.6×10-5mol/L
5.6×10-5mol/L
.(2011?河西区一模)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,现进行如下实验,在体积为l L的密闭容器中,充入1molCO2和3.25molH2,一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的浓度随时问变化如图所示.

①写出该工业方法制取甲醇的化学方程式:
②从反应开始到平衡,氢气的平均反应速率v(H2)=
③该条件下反应的平衡常数K的值为
④下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g)
C.将H2O(g)从体系中分离 D.用更有效的催化剂
(2)在载人航天器的生态系统中.不仅要求分离除去CO2还要求提供充足的O2?某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料.已知该反应的阳极反应为4OH--4e-=O2↑+2H2O.划阴极反应式为:
查看习题详情和答案>>
(1)目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,现进行如下实验,在体积为l L的密闭容器中,充入1molCO2和3.25molH2,一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的浓度随时问变化如图所示.

①写出该工业方法制取甲醇的化学方程式:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
. CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)②从反应开始到平衡,氢气的平均反应速率v(H2)=
0.225
0.225
mol/(L?min).平衡时CO2的转化事为75%
75%
.③该条件下反应的平衡常数K的值为
2.25
2.25
.当温度降低时K值变大,剐该反应的△H<
<
0(填“<”、“>”或“=”)④下列措施中能使n(CH3OH)/n(CO2)增大的是
C
C
.A.升高温度 B.充入He(g)
C.将H2O(g)从体系中分离 D.用更有效的催化剂
(2)在载人航天器的生态系统中.不仅要求分离除去CO2还要求提供充足的O2?某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料.已知该反应的阳极反应为4OH--4e-=O2↑+2H2O.划阴极反应式为:
2CO2+4e-+2H2O=2CO+4OH-
2CO2+4e-+2H2O=2CO+4OH-
. (2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.
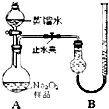
(2011?宁德一模)某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究.[实验一]取样品0.100g,用如图所示实验装置进行测定.(夹持装置省略)
(1)检查装置A气密性的方法是
夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好;或者关闭分液漏斗活塞,右侧的导管插入水中,用手捂住分液漏斗,看是否有气泡产生,冷却后是否有一段水柱形成
夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好;或者关闭分液漏斗活塞,右侧的导管插入水中,用手捂住分液漏斗,看是否有气泡产生,冷却后是否有一段水柱形成
.(2)若在实验过程中共产生气体11.20mL(已折算成标准状况),则样品中Na2O2的纯度为
78%
78%
.[实验二]样品溶于水后用盐酸滴定
(3)取一定量样品溶于水并稀释至250mL,配制时,所用到的玻璃仪器除了烧杯和玻璃棒外,还需用到
250 mL容量瓶、胶头滴管
250 mL容量瓶、胶头滴管
.(4)取上述所配溶液各25.00mL,用一定浓度的标准盐酸滴定,平行实验记录如下表:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 标准盐酸体积(mL) | 23.00 | 24.98 | 25.00 | 25.02 |
25.00
25.00
mL.若滴定前用上述所配溶液润洗锥形瓶,对实验测定结果产生的影响是偏高
偏高
(填“偏高”、“偏低”或“无影响”).[实验分析]实验结果对比分析
(5)小组同学对比两个实验发现,实验一测得的Na2O2样品的纯度比理论值明显偏小.经过分析,小组同学认为,明显偏差不是由操作失误和装置缺陷引起的,可能是反应原理上的原因.查阅资料发现:Na2O2与水反应产生的H2O2未完全分解.
①写出Na2O2与水生成H2O2的化学方程式
Na2O2+2H2O=2NaOH+H2O2
Na2O2+2H2O=2NaOH+H2O2
.②若将实验一稍加改进,就能使测定结果接近理论值,写出改进方案:
反应前向Na2O2样品中加入少量MnO2
反应前向Na2O2样品中加入少量MnO2
.