网址:http://m.1010jiajiao.com/timu3_id_340812[举报]
(14分)已知CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数随温度变化如下表:
CO(g)+H2O(g)的平衡常数随温度变化如下表:
|
t/℃ |
700 |
800 |
850 |
1 000 |
1 200 |
|
K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
请回答下列问题:
(1)上述正向反应是________反应(选填“放热”或“吸热”)。
(2)若达平衡后降温,则平衡向________移动,CO2转化率________,正反应速率________(选填“增大”、“减小”或“不变”)。
(3)在850℃发生上述反应,以表中的物质的量投入恒容反应器中,其中向正反应方向移动的有________(选填A、B、C、D、E)
|
|
A |
B |
C |
D |
E |
|
n(CO2) |
3 |
1 |
0 |
1 |
1 |
|
n(H2) |
2 |
1 |
0 |
1 |
2 |
|
n(CO) |
1 |
2 |
3 |
0.5 |
3 |
|
n(H2O) |
5 |
2 |
3 |
2 |
1 |
(4)在850℃时,可逆反应:CO2(g)+H2(g) CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
|
时间/min |
CO2 (mol/L) |
H2 (mol/L) |
CO (mol/L) |
H2O (mol/L) |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
则3 min~4 min平衡后c3=______________,CO2的转化率为____________。
查看习题详情和答案>>
乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH CH3COOC2H5+H2O

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;
②部分有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.5 | 78.5 | 117.9 | 77 |
请回答下列问题:
(1)浓硫酸的作用是 ,球形干燥管的作用是 。
(2)用如图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为 、 等。
(3)实验所得到的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,除去 ;再进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
同一反应时间 | 同一反应应温度 | ||||
反应温度/℃ | 转化率(%) | 选择性(%)* | 反应时间/h | 转化率(%) | 选择性(%)* |
40 | 77.8 | 100 | 2 | 80.2 | 100 |
60 | 92.3 | 100 | 3 | 87.8 | 100 |
80 | 92.6 | 100 | 4 | 92.3 | 100 |
120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
*选择性100%表示反应生成的产物全部是乙酸乙酯和水 | |||||
①根据表中数据,下列 (填字母)为该反应的最佳条件。
a.120℃,4h b.80℃,2h c.60℃,4h d.40℃,3h
②当反应温度达到120℃时,反应选抒性降低的原因可能为 。
查看习题详情和答案>>(14分)已知CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数随温度变化如下表:
| t/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
请回答下列问题:
(1)上述正向反应是________反应(选填“放热”或“吸热”)。
(2)若达平衡后降温,则平衡向________移动,CO2转化率________,正反应速率________(选填“增大”、“减小”或“不变”)。
(3)在850℃发生上述反应,以表中的物质的量投入恒容反应器中,其中向正反应方向移动的有________(选填A、B、C、D、E)
|
| A | B | C | D | E |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
(4)在850℃时,可逆反应:CO2(g)+H2(g)CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O (mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
则3 min~4 min平衡后c3=______________,CO2的转化率为____________。
查看习题详情和答案>>
(共9分) (1) 谷氨酸的系统名为:2-氨基戊二酸(pKa1=2.19,pKa2=4.25,pKa3=9.67)。请回答下列问题:
① 写出其结构式 ;
② 写出谷氨酸在pH=10.00的水溶液中,占优势的离子结构 ;
③ 若谷氨酸溶于pH=7的纯水中,所得溶液的pH是x,则x 7(填“>”或“<”);此氨基酸等电点是大于x还是小于x?为什么?
。
(2) 110.1℃,6.050×104Pa,测定醋酸蒸气的密度所得到的平均相对摩尔质量是醋酸单分子摩尔质量的1.520倍。假定气体中只含有单分子和双分子。则110.1℃下反应2CH3COOH(g)![]() (CH3COOH)2(g)的
(CH3COOH)2(g)的![]() 为 ;
为 ;![]() 的计算公式及结果为:(
的计算公式及结果为:(![]() =1.013×105Pa) 。
=1.013×105Pa) 。
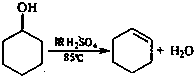
实验步骤下:
①在25mL干燥的圆底烧瓶中加入10g环己醇和0.5mL 98%浓硫酸,充分振荡.
②向烧瓶中放入2~3粒沸石,安装分馏装置,接收瓶用冰水冷却.
③小心加热,控制加热速度使温度不超过90℃,直到瓶底剩余少量残渣并出现白雾时停止加热.(已知:环己烯,沸点82.98℃;环己烯-10%水,沸点70.8℃;环己醇-80%水,沸点97.8℃:环己醇-30.5%环己烯,沸点64.9℃)
④向馏出液中加约1g精盐使其达饱和,然后加入2mL饱和碳酸钠水溶液,充分振荡.
⑤…
⑥有机层倒入干燥的小锥形瓶中,加入1~2g无水氯化钙干燥.待溶液清亮透明后过滤.
⑦将滤液移入圆底烧瓶中,加入2~3粒沸石,蒸馏.收集80~85℃馏分,称重约7.4g.
⑧计算.
请回答下列问题:
(1)步骤①中,加入10g环已醇和0.5mL 98%浓硫酸的顺序是
(2)步骤③中,为便干控制加热温度,应该采取的加热方法是
(3)步骤④中,向馏出液中加约1g精盐使其达饱和的目的是
(4)步骤⑤的操作是
(5)步骤⑧计算得到的环己烯的产率为