摘要:9.室温时.0.01mol/L某一元弱酸HA中,有1%的HA发生了电离.则下列说法正确的是 (A)上述弱酸溶液的pH=4 (B)加入等体积的0.01mol/LNaOH溶液后.所得溶液的pH=7 (C)加入等体积的0.01mol/LNaOH溶液后.所得溶液的pH>7 (D)加入等体积的0.01mol/LNaOH溶液后.所得溶液的pH<7
网址:http://m.1010jiajiao.com/timu3_id_34052[举报]
I.常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示。回答下列问题

(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是___________________。
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点……
指示剂B的变色范围在pH=______左右最理想。
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是____________________。
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=2×10-4,当溶液中c(HCO3-)︰c(CO32-)=
2︰1时,溶液的pH=_____________。
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A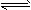 H++HA- HA-
H++HA- HA-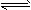 H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)> α(HA-),设有下列四种溶液:
(A)0.01mol/L 的H2A溶液
(B)0.01mol/L 的NaHA溶液
(C)0.01mol/L 的HCl与0.04mol/L的NaHA溶液等体积混合液
(D)0.02mol/L 的NaOH与0.02 mol/L的NaHA溶液等体积混合液
据此,填写下列空白(填代号) :
(5)c(H+)最大的是_________,c(H2A)最大的是___________,c(A2-)最大的是_________。
查看习题详情和答案>>
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点……
指示剂B的变色范围在pH=______左右最理想。
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是____________________。
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=2×10-4,当溶液中c(HCO3-)︰c(CO32-)=
2︰1时,溶液的pH=_____________。
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A
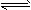 H++HA- HA-
H++HA- HA-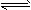 H++A2-
H++A2-已知相同浓度时的电离度α(H2A)> α(HA-),设有下列四种溶液:
(A)0.01mol/L 的H2A溶液
(B)0.01mol/L 的NaHA溶液
(C)0.01mol/L 的HCl与0.04mol/L的NaHA溶液等体积混合液
(D)0.02mol/L 的NaOH与0.02 mol/L的NaHA溶液等体积混合液
据此,填写下列空白(填代号) :
(5)c(H+)最大的是_________,c(H2A)最大的是___________,c(A2-)最大的是_________。
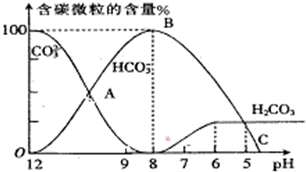 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是______.
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=______左右最理想.
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是______.
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=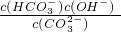 =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A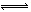 H++HA- HA-
H++HA- HA- H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是______,c(H2A)最大的是______,c(A2-)最大的是______.
查看习题详情和答案>>
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是______.
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=______左右最理想.
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是______.
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh= =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A H++HA- HA-
H++HA- HA- H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是______,c(H2A)最大的是______,c(A2-)最大的是______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是______.
(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=______左右最理想.
(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是______.
(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=
 =2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.
=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=______.II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A
 H++HA- HA-
H++HA- HA- H++A2-
H++A2-已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是______,c(H2A)最大的是______,c(A2-)最大的是______.
 查看习题详情和答案>>
查看习题详情和答案>>
 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:(1)H2CO3、HCO3-、CO32-中不能大量共存于同一溶液中的是
H2CO3、CO32-
H2CO3、CO32-
.(2)实验室可用“双指示剂法”测定碳酸钠、碳酸氢钠混合溶液中各种物质的含量,操作步骤如下:
①取固体样品配成溶液;
②取25mL样品溶液加指示剂A,用0.1010mol/LNaOH标准溶液滴定至终点;
③再加指示剂B,再用0.1010mol/LNaOH标准溶液滴定至终点…
指示剂B的变色范围在pH=
4.5
4.5
左右最理想.(3)当pH=7时,此时再滴入盐酸溶液所发生反应离子方程式是
HCO3-+H+=H2CO3
HCO3-+H+=H2CO3
.(4)已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=
c(
| ||
c(
|
10
10
.II.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A
 H++HA- HA-
H++HA- HA- H++A2-
H++A2-已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(5)c(H+)最大的是
A
A
,c(H2A)最大的是C
C
,c(A2-)最大的是D
D
.