摘要:如图表示反应A2+B22AB在不同温度和压强改变的条件下产物AB的物质的量随时间的变化关系.a为500℃时的情况,b为300℃时的情况,c为反应在300℃时从时间t3开始向容器中加压的情况.则下列叙述正确的是 A.A2.B2及AB均为气体.△H<0 B.AB为气体.A2.B2中至少有一种为非气体.△H<0 C.AB为气体.A2.B2中有一种为非气体.△H>0 D.AB为固体.A2.B2中有一种为非气体.△H<0
网址:http://m.1010jiajiao.com/timu3_id_338214[举报]
 A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:(1)将E的单质投入水中,发生反应的离子方程式为
2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
该反应的氧化剂是H2O
H2O
.(2)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是
10-4:1
10-4:1
.(3)化学反应3A2(g)+C2(g)?2CA3(g).△H=-92.4kJ?mol-1
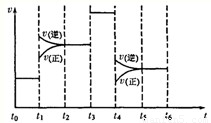
①当反应达到平衡时不断改变条件(不改变A2、C2和CA3的 量),如图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是
t0~t1
t0~t1
.②温度为T℃时,将5mol A2和2mol C2放入0.5L密闭容器中,平衡后测得C2的转化率为50%,计算反应的平衡常数为
0.125
0.125
.(4)已知0.4mol 液态C2 A4与液态双氧水反应,生成C2和液态水,放出327.2kJ的热量.1mol液态水变为水蒸气需吸收44.0kJ的热量.写出液态C2 A4与液态双氧水反应,生成C2和水蒸气的热化学方程式
N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-642kJ?mol-1
N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-642kJ?mol-1
.
A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)将E的单质投入水中,发生反应的离子方程式为______该反应的氧化剂是______.
(2)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是______.
(3)化学反应3A2(g)+C2(g)?2CA3(g).△H=-92.4kJ?mol-1
①当反应达到平衡时不断改变条件(不改变A2、C2和CA3的 量),如图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是______.
②温度为T℃时,将5mol A2和2mol C2放入0.5L密闭容器中,平衡后测得C2的转化率为50%,计算反应的平衡常数为______.
(4)已知0.4mol 液态C2 A4与液态双氧水反应,生成C2和液态水,放出327.2kJ的热量.1mol液态水变为水蒸气需吸收44.0kJ的热量.写出液态C2 A4与液态双氧水反应,生成C2和水蒸气的热化学方程式______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)将E的单质投入水中,发生反应的离子方程式为______该反应的氧化剂是______.
(2)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是______.
(3)化学反应3A2(g)+C2(g)?2CA3(g).△H=-92.4kJ?mol-1
①当反应达到平衡时不断改变条件(不改变A2、C2和CA3的 量),如图表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是______.
②温度为T℃时,将5mol A2和2mol C2放入0.5L密闭容器中,平衡后测得C2的转化率为50%,计算反应的平衡常数为______.
(4)已知0.4mol 液态C2 A4与液态双氧水反应,生成C2和液态水,放出327.2kJ的热量.1mol液态水变为水蒸气需吸收44.0kJ的热量.写出液态C2 A4与液态双氧水反应,生成C2和水蒸气的热化学方程式______.
 查看习题详情和答案>>
查看习题详情和答案>>
 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题:(1)某溶液含两种相同物质的量的溶质,且其中只存在OH一、H+、N
| H | + 4 |
| H | + 4 |
NH4Cl和NH3?H2O
NH4Cl和NH3?H2O
.(2)0.1mol?L-1的氨水与0.05mol?L-1的稀硫酸等体积混合,用离子方程式表示混合后溶液的酸碱性:
NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
. NH3?H2O+H+
NH3?H2O+H+(3)已知:Ksp(RX)=1.8×10-10,Ksp(RY)=1.5×10-16,Ksp(R2Z)=2.0×10-12,则难溶盐RX、RY和R2Z的饱和溶液中,R+浓度由大到小的顺序是
R2Z>RX>RY
R2Z>RX>RY
.(4)以石墨电极电解100mL 0.1mol?L-1CuSO4溶液.若阳极上产生气体的物质的量为0.01mol,则阴极上析出Cu的质量为
0.64
0.64
g.(5)向20mL硫酸和盐酸的混合液中逐滴加入pH=13的Ba(OH)2溶液,生成BaSO4的量如图所示,B点溶液的pH=7(假设体积可以直接相加),则c(HCl)=
0.2
0.2
mol?L-1.(6)在温度、容积相同的3个密闭容器中,按下表投入反应物,发生反应(H2(g)+
I2(g)?2HI(g)△H=-14.9kJ?mol-1),在恒温、恒容条件下,测得反应达
到平衡时的数据如下表:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol H2、1mol I2 | 2 mol HI | 4 mol HI |
| HI的浓度(mol?L-1) | C1 | C2 | C3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 反应物转化率 | a1 | a2 | a3 |
AC
AC
.A.α1+α2=1 B.2α2=α3 C.a+b=14.9 D.c1=c2=c3.
 A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:
A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:(1)C在元素周期表中的位置为
(2)F单质的燃烧热△H=-akJ/mol,写出表示F单质的燃烧热的热化学方程式
(3)E单质与D的最高价氧化物的水化物的溶液反应的离子方程式为
(4)A、B两元素可形成离子化合物BA5,其电子式为
(5)将0.4mol FC2和0.2mol C2放入容积为2L的_密闭容器中,在一定条件下发生 反应2FC2+C2?2FC3,当FC2百分含量不变时,得到0.2mol FC3气体,则此时反应的平衡常数K=
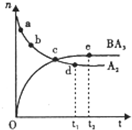
(6)向一绝热恒容密闭容器中通入B2和A2,在一定条件下发生反应B2(g)+3A2(g)?2BA3(g)△H<0,达到平衡,n(A2)和n(BA3)随时间变化的关系如图所示.下列有关叙述一定正确的是
A.c点表示BA3生成速率与BA3分解速率相等
B.c点和e点 A2的转化率相等
C.平衡后再升高温度,不利于BA3的合成
D.d点时:n(A2):n(BA3)=3:2
(7)将E元素的单质(除去氧化膜)投入浓的氯化铜溶液中,在其表面很 快出现一层红色物质,产生气体的速率逐渐加快,经检验,该气体为氢气,用温度计测得溶液的温度迅速升高.请从有关能量、是否有电化学作用等方面,分析能产生氢气且开始 阶段的速率不断加快的原因
 在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,回答下列问题:
在一定条件下,可逆反应A+B?mC变化如图所示.已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况,回答下列问题:(1)温度T1
>
>
T2(填“>”“=”或“<”).(2)正反应是
放热
放热
反应(填“吸热”或“放热”).(3)如果A、B、C均为气体,则m
>
>
2(填“>”“=”或“<”).(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强
增大
增大
(填“增大”“减小”或“不变”),平衡不
不
移动(填“向正反应方向”“向逆反应方向”或“不”).(5)已知2A(g)+B(g)?2C(g)△H=-a kJ?mol-1(a>0),在一个有催化剂的固定容积的容器中加入2mol A和1mol B,在500℃时充分反应达平衡后C的浓度为ω mol/L,放出热量b kJ.
①a
>
>
b(填“>”“=”或“<”).②若将反应温度升高到700℃,该反应的平衡常数将
减小
减小
(填“增大”“减小”或“不变”).③在上述容器中为使该反应的反应速率增大,且平衡向正反应方向移动的可采取的措施是
增大A2的浓度,或增大B2的浓度或同时增大A2、B2的浓度
增大A2的浓度,或增大B2的浓度或同时增大A2、B2的浓度
(说出一种即可)