网址:http://m.1010jiajiao.com/timu3_id_337752[举报]
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯、二甲苯等有害物质可转化为二氧化碳和水,达到无害化.有关甲醛、苯、二甲苯、二氧化碳及水说法正确的是
A.苯与B3N3H6互为等电子体,分子中原子共平面,且都有三种二氯代物;
B.二氧化碳、甲醛、氯仿(CHCl3)中碳原子分别采用sp、sp2、sp3杂化;
C.对二甲苯是非极性分子,邻二甲苯和间二甲苯都是极性分子;
D.氨比甲醛易溶于水,是因为甲醛与水分子间不能形成氢键.
(3)日常生活中广泛使用的不锈钢就是含铬合金,铬元素原子中末成对电子数为
(4)①短周期某主族元素M的逐级电离能情况如下图A所示,则M元素形成化合物时,表现的主要化合价为
②第三周期八种元素按单质熔点高低的顺序如下图B所示,其中序号“8”代表

(5)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.科学家把C60和K掺杂在一起制造了一种富勒烯
 化合
化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质的K原子和C60分子的个数比为
(6)在配合物Fe(SCN)2+离子中,提供空轨道接受孤对电子的微粒是
 确定物质性质的重要因素是物质结构.请回答下列问题.
确定物质性质的重要因素是物质结构.请回答下列问题.(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A的第一电离能
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示,其中TiN中N呈-3价),已知3种离子晶体的晶格能数据如下表:
| 离子晶体 | KCl | MgO | CaO |
| 晶格能/kJ?mol-1 | 715 | 3791 | 3401 |
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(4)某配合物的分子结构如图2所示,其分子内不含有
A.离子键 B.极性键 C.金属键
D.配位键 E.氢 键 F.非极性键
(5)某离子X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如右图所示.X的元素符号是
(6)在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构.则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是
A.SP,范德华力 B.sp2,范德华力 C.sp2,氢键 D.sp3,氢键
(7)CaC2中
| C | 2- 2 |
| O | 2+ 2 |
| O | 2+ 2 |


| O | 2+ 2 |
 (2013?德州一模)【化学一物质结构与性质】
(2013?德州一模)【化学一物质结构与性质】A-E是周期表中1一36号的元素,它们的原子序数依次递增且分别位于前四周期的各个 周期中.对它们的性质及结构的描述如下.
A原子的基态只有一种形状的电子云,并容易形成共价键;B原子的最外电子层的电子排 布可表示为nsnnpn,其元素最高正化合价与最低负化合价的代数和为0;C与B同周期,其 第一电离能髙于周期表中与之相邻的所有元素;D元素在周期表中位于C元素的下一周 期,其电负性在同周期元素中最大;E原子最外电子层只有未成对电子,其内层所有轨道全 部充满,但并不是第IA族元素.
(1)请写出E原子基态的电子排布式
(2)A与C形成的最简单化合物(甲)分子的立体结构是
(3)A与D元素形成的化合物(乙)与甲相比,沸点较低的是(写化学式)
(4)B元素可形成B70单质,它在一定条件下吸收可见光后可高效 杀灭癌细胞,有望成为癌症治疗药物的候选材料.它与金属钾掺杂在一起的化合物,其晶胞如图所示(白球位于立方体的体心和顶 点,小黑球位于立方体的面上),则该化合物中B70与钾原子个数比为
(12分)过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
Ⅰ. 二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A.苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
Ⅱ. 2007年诺贝尔物理学奖为法国科学家阿尔贝·费尔和德国科学家彼得·格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就。某钙钛型复合氧化物(如右图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。
(1)用A、B、O表示这类特殊晶体的化学式: 。
(2)已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3, (x < 0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为: 。(用含x的代数式表示)
(3)Mn的外围电子轨道表示式为: 。
(4)下列有关说法正确的是 。
A.镧、锰、氧分别位于周期表f、d、p区
B.氧的第一电离能比氮的第一电离能大
C.铬的堆积方式与钾相同,则其堆积方式如右图:
D.锰的电负性为1.59 ,Cr的电负性为1.66,说明锰的金属性比铬强
金属镁有许多重要的用途,法国化学家维多克·格利雅因发明了在有机合成方面用途广泛的格利雅试剂而荣获诺贝尔化学奖,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图: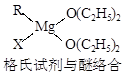
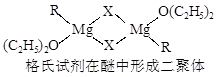
①标出格氏试剂 中的配位键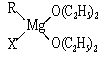
②下列比较中正确的是
A.金属键的强弱:Mg>Al B.基态原子第一电离能:Mg>Al
C.金属性:Mg>Al D.晶格能:KCl>NaCl
E.电负性:Mg>Al F.硬度:Mg>Al 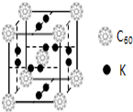
③二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A.苯与B3N3H6互为等电子体
www.kB.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键