网址:http://m.1010jiajiao.com/timu3_id_337360[举报]
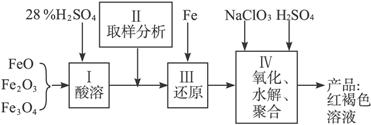
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有_______;
A.容量瓶 B.烧杯 C.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_________;
A.控制溶液中Fe2+与Fe3+含量比 B.确定下一步还原所需铁的量
C.确定氧化Fe2+所需NaClO3的量 D.确保铁的氧化物酸溶完全
(3)用NaClO3氧化时反应方程式如下:
6FeSO4+NaClO3+3H2SO4====3Fe2(SO4)3+NaCl+3H2O
若改用HNO3氧化,则反应方程式如下:
6FeSO4+2HNO3+3H2SO4====3Fe2(SO4)3+2NO↑+4H2O
已知1 mol HNO3价格0.16元、1 mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的利弊。利是______________________,弊是______________________;
聚合硫酸铁溶液中![]() 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中![]() 与Fe3+物质的量之比。
与Fe3+物质的量之比。
(4)测定时所需的试剂为_________;
A.NaOH B.FeSO4 C.BaCl2 D.NaClO3
(5)需要测定________和_________的质量(填写化合物的化学式);
(6)选出测定过程中所需的基本操作__________(按操作先后顺序列出)。
A.萃取、分液 B.过滤、洗涤 C.蒸发、结晶
D.冷却、称量 E.烘干或灼烧
查看习题详情和答案>>
请完成下列各题:
(1)写出反应类型:反应①
(2)写出反应条件:反应③
(3)反应②③的目的是:
(4)写出反应⑤的化学方程式:
(5)B被氧化成C的过程中会有中间产物生成,该中间产物可能是
(6)写出G的结构简式


(1)制备皓矾的实验流程如图所示.
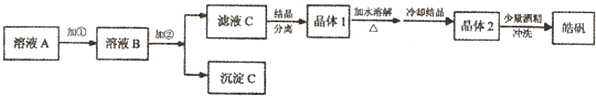
已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:
Fe(OH)3:2.7一3.7
Fe(OH)2:7.6一9.6
Zn(OH)2:5.7一8.0
试回答下列问题:①加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,应选用
②加入的试剂②,供选择使用的有:Zn粉、ZnO、Zn(OH)2、ZnCO3、ZnSO4等,应选用
③从晶体1→晶体2,该过程的名称是
④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
(2)探究ZnSO4?7H2O的性质
⑤称取28.7g ZnSO4?7H2O研细后置于坩埚中小心加热,测得残留固体的质量与温度的对应数据见下表:
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
| ||
| ||
⑥取少量ZnSO4?7H2O配成溶液向其中逐滴加入NaOH溶液,发现先产生白色沉淀后又逐渐溶解;若改用氨水得到相同的现象.查资料知,氢氧化锌与氢氧化铝均有两性,且锌离子可与氨水形成络合离子[Zn(NH3)4]2+.则Zn(OH)2沉淀中加入NaOH溶液和加氨水均得到无色溶液的离子反应方程式为:

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7Fe(OH)2:7.6-9.6 Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用
(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用
(3)从晶体1→晶体2,该过程的名称是
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是