摘要:10.某一元弱酸HA的电离度为a.则浓度为1 mol·L-1的HA溶液中.H+离子.A-离子和未电离的HA分子的总个数是阿伏加德罗常数的 [ ] A.a倍 B.(1-a)倍 C.(1+a)倍 D.2a倍
网址:http://m.1010jiajiao.com/timu3_id_33556[举报]
某一元弱酸HA的电离度为a,则浓度为1 mol·L-1的HA溶液中,H+离子、A-离子和未电离的HA分子的总个数是阿伏加德罗常数的
A.a倍
B.(1-a)倍
C.(1+a)倍
D.2a倍
查看习题详情和答案>>某一元弱酸HA的电离度为a,则浓度为1 mol·L-1的HA溶液中,H+离子、A-离子和未电离的HA分子的总个数是阿伏加德罗常数的
| A.a倍 |
| B.(1-a)倍 |
| C.(1+a)倍 |
| D.2a倍 |
将某一元酸HA溶液与NaOH溶液等体积混合:
(1)若c (HA)=c (NaOH)=0.1mol/L,测得混合后溶液的pH>7.
①不能证明HA是弱电解质的方法是
A.测得0.1mol/L HA的pH>l
B.测得NaA溶液的pH>7
C.pH=l的HA溶液与盐酸,稀释100倍后,盐酸的pH变化大
D.用足量锌分别与相同pH、相同体积的盐酸和HA溶液反应,产生的氢气一样多
②混合溶液中,关系式一定正确的是
A.c(A-)>c(Na+)>c(OH-)>c(H+) B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L D.c( HA)+c( H+)=c(OH-)
③若HA+B2-(少量)=A-+HB-、H2B(少量)+2C-=B2-+2HC、HA+C-=A-+HC,则相同pH的 ①NaA溶液 ②Na2B溶液 ③NaHB溶液 ④NaC溶液,其物质的量浓度由大到小的顺序为
(2)若c( HA)=c(NaOH)=0.1mol/L,测得混合后溶液的pH=7.
①现将一定浓度的HA溶液和0.1mol/L NaOH溶液等体积混合后,所得溶液的pH跟该浓度的HA溶液稀释10倍后所得溶液的pH相等,则HA溶液的物质的量浓度为
②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏大的是
A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数
(3)若c(HA)=0.04mol/L,c(NaOH)═0.02mol/L.
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)
②若HA为CH3COOH,该溶液显酸性,溶液中所有离子按浓度由大到小排列的顺序是
③若HA为强酸,99℃时(Kw=10-12),将两种溶液等体积混合后,溶液中由水电离出的H+浓度为
查看习题详情和答案>>
(1)若c (HA)=c (NaOH)=0.1mol/L,测得混合后溶液的pH>7.
①不能证明HA是弱电解质的方法是
D
D
A.测得0.1mol/L HA的pH>l
B.测得NaA溶液的pH>7
C.pH=l的HA溶液与盐酸,稀释100倍后,盐酸的pH变化大
D.用足量锌分别与相同pH、相同体积的盐酸和HA溶液反应,产生的氢气一样多
②混合溶液中,关系式一定正确的是
BD
BD
A.c(A-)>c(Na+)>c(OH-)>c(H+) B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L D.c( HA)+c( H+)=c(OH-)
③若HA+B2-(少量)=A-+HB-、H2B(少量)+2C-=B2-+2HC、HA+C-=A-+HC,则相同pH的 ①NaA溶液 ②Na2B溶液 ③NaHB溶液 ④NaC溶液,其物质的量浓度由大到小的顺序为
③>①>②>④
③>①>②>④
(填序号).(2)若c( HA)=c(NaOH)=0.1mol/L,测得混合后溶液的pH=7.
①现将一定浓度的HA溶液和0.1mol/L NaOH溶液等体积混合后,所得溶液的pH跟该浓度的HA溶液稀释10倍后所得溶液的pH相等,则HA溶液的物质的量浓度为
0.125mol/L
0.125mol/L
.②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏大的是
ABC
ABC
.A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数
(3)若c(HA)=0.04mol/L,c(NaOH)═0.02mol/L.
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)
大于
大于
c (CN-)(填“小于”、“等于”或“大于”),得出该结论的依据是因为c(Na+)+c(H+)=c(CN-)+c(OH-),溶液呈碱性,则c(H+)<c(OH-),所以c(Na+)>c(CN-)
因为c(Na+)+c(H+)=c(CN-)+c(OH-),溶液呈碱性,则c(H+)<c(OH-),所以c(Na+)>c(CN-)
.②若HA为CH3COOH,该溶液显酸性,溶液中所有离子按浓度由大到小排列的顺序是
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
.③若HA为强酸,99℃时(Kw=10-12),将两种溶液等体积混合后,溶液中由水电离出的H+浓度为
10-10
10-10
mol/L(假设混合后溶液体积为两溶液体积之和).将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
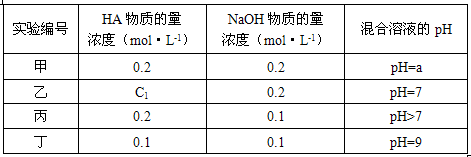
请回答:
(1)不考虑其它组的实验结果,单从甲组情况分析,若a_________7(填>、<或=),则HA为弱酸。
(2)在乙组中混合溶液中离子浓度 (A-)与 (Na+)的大小关系是___________。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是__________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是_____________ 。
(4)丁组实验所得混合溶液中由水电离出的 =___________ mol·L-1。
查看习题详情和答案>>
(1)不考虑其它组的实验结果,单从甲组情况分析,若a_________7(填>、<或=),则HA为弱酸。
(2)在乙组中混合溶液中离子浓度 (A-)与 (Na+)的大小关系是___________。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是__________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是_____________ 。
(4)丁组实验所得混合溶液中由水电离出的 =___________ mol·L-1。
将某一元酸HA溶液与NaOH溶液等体积混合:
(1)若c (HA)=c (NaOH)=0.lmol/L,测得混合后溶液的pH>7.
①不能证明HA是弱电解质的方法是______
A.测得0.1mol/L HA的pH>l
B.测得NaA溶液的pH>7
C.pH=l的HA溶液与盐酸,稀释100倍后,盐酸的pH变化大
D.用足量锌分别与相同pH、相同体积的盐酸和HA溶液反应,产生的氢气一样多
②混合溶液中,关系式一定正确的是______
A.c(A-)>c(Na+)>c(OH-)>c(H+) B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L D.c( HA)+c( H+)=c(OH-)
③若HA+B2-(少量)=A-+HB-、H2B(少量)+2C-=B2-+2HC、HA+C-=A-+HC,则相同pH的 ①NaA溶液 ②Na2B溶液 ③NaHB溶液 ④NaC溶液,其物质的量浓度由大到小的顺序为______(填序号).
(2)若c( HA)=c(NaOH)=0.1mol/L,测得混合后溶液的pH=7.
①现将一定浓度的HA溶液和0.1mol/L NaOH溶液等体积混合后,所得溶液的pH跟该浓度的HA溶液稀释10倍后所得溶液的pH相等,则HA溶液的物质的量浓度为______.
②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏大的是______.
A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数
(3)若c(HA)=0.04mol/L,c(NaOH)═0.02mol/L.
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)______c (CN-)(填“小于”、“等于”或“大于”),得出该结论的依据是______.
②若HA为CH3COOH,该溶液显酸性,溶液中所有离子按浓度由大到小排列的顺序是______.
③若HA为强酸,99℃时(Kw=10-12),将两种溶液等体积混合后,溶液中由水电离出的H+浓度为______mol/L(假设混合后溶液体积为两溶液体积之和).
查看习题详情和答案>>
(1)若c (HA)=c (NaOH)=0.lmol/L,测得混合后溶液的pH>7.
①不能证明HA是弱电解质的方法是______
A.测得0.1mol/L HA的pH>l
B.测得NaA溶液的pH>7
C.pH=l的HA溶液与盐酸,稀释100倍后,盐酸的pH变化大
D.用足量锌分别与相同pH、相同体积的盐酸和HA溶液反应,产生的氢气一样多
②混合溶液中,关系式一定正确的是______
A.c(A-)>c(Na+)>c(OH-)>c(H+) B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L D.c( HA)+c( H+)=c(OH-)
③若HA+B2-(少量)=A-+HB-、H2B(少量)+2C-=B2-+2HC、HA+C-=A-+HC,则相同pH的 ①NaA溶液 ②Na2B溶液 ③NaHB溶液 ④NaC溶液,其物质的量浓度由大到小的顺序为______(填序号).
(2)若c( HA)=c(NaOH)=0.1mol/L,测得混合后溶液的pH=7.
①现将一定浓度的HA溶液和0.1mol/L NaOH溶液等体积混合后,所得溶液的pH跟该浓度的HA溶液稀释10倍后所得溶液的pH相等,则HA溶液的物质的量浓度为______.
②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏大的是______.
A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数
(3)若c(HA)=0.04mol/L,c(NaOH)═0.02mol/L.
①若HA为HCN,该溶液显碱性,则溶液中c(Na+)______c (CN-)(填“小于”、“等于”或“大于”),得出该结论的依据是______.
②若HA为CH3COOH,该溶液显酸性,溶液中所有离子按浓度由大到小排列的顺序是______.
③若HA为强酸,99℃时(Kw=10-12),将两种溶液等体积混合后,溶液中由水电离出的H+浓度为______mol/L(假设混合后溶液体积为两溶液体积之和).