摘要:2.中有关物质结构部分的内容还有: (1)理解离子键.共价键的涵义.理解极性键和非极性键.了解极性分子和非极性分子.了解分子间作用力.初步了解氢键.能用有关原理解释一些实际问题. (2)了解几种晶体类型(离子晶体.原子晶体.分子晶体和金属晶体)及其性质.了解各类晶体内部微粒间的相互作用.能够根据晶体的性质判断晶体类型等. (3)能对原子.分子.化学键等微观结构进行三维空间想像.重视理论联系实际.用物质结构理论解释一些具体问题. 高考试题中常常是结合元素化合物内容进行综合考查.题型上看可以是选的择题.简答题.填空题等.
网址:http://m.1010jiajiao.com/timu3_id_333661[举报]
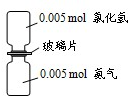 如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )| A、气体反应物的总体积为0.224L | B、产物中所含的N-H键个数为0.015NA | C、生成物的物质的量为0.005mol | D、加水溶解后所得溶液中NH4+浓度为0.005mol?L-1 |
 已知反应:3I-(aq)+
已知反应:3I-(aq)+| S 2O | 2- 8 |
- 3 |
| 2SO | 2- 4 |
(1)写出反应的平衡常数表达式K=
c
| ||||
c3(I-)?c
|
c
| ||||
c3(I-)?c
|
(2)如图表示反应过程中有关物质的能量,则反应的△H
<
<
0(填“>”、“<”或“=”);(Ⅰ)、(Ⅱ)两线中,使用催化剂的是
(Ⅱ)
(Ⅱ)
线;(3)反应中发生反应的I-与被氧化的I-的物质的量比为
3:2
3:2
;(4)反应的速率可以用
| I | - 3 |
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ||
| c(I-)/mol?L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 | ||
c(
|
0.040 | 0.040 | 0.080 | 0.080 | 0.040 | ||
| t/s | 88 | 44 | 22 | 11 | t1 |
研究反应物I-与S2O82-的浓度对反应速率的影响
研究反应物I-与S2O82-的浓度对反应速率的影响
,显色时间t1=22
22
s,分析表中数据,得出的结论是反应速率与反应物起始浓度乘积成正比
反应速率与反应物起始浓度乘积成正比
.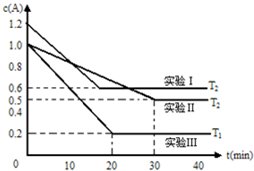 恒容体系,发生如下反应2A(g)?B(g)+xC(?)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图(某课外活动小组一共进行了如图所示的三个实验,其中T1、T2表示不同的反应温度):
恒容体系,发生如下反应2A(g)?B(g)+xC(?)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图(某课外活动小组一共进行了如图所示的三个实验,其中T1、T2表示不同的反应温度):(1)在实验Ⅲ中,0~20min的时间内,v(B)=
0.02mol/(L.min)
0.02mol/(L.min)
.(2)根据以上实验事实,完成以下填空:x=
1
1
,生成物C的状态为气态
气态
,反应热△H>
>
0(填“>”、“=”或者“<”).(3)在实验Ⅱ中,当化学反应进行到35min时,下列关于反应体系中的有关说法,正确的是
abde
abde
.a.单位时间内生成n mol B的同时生成2n mol A
b.单位时间内生成n mol C的同时消耗2n mol A
c.用A、B、C表示的反应速率的比为2:1:2
d.混合气体中反应物A与生成物B的体积分数之比为2:1
e.混合气体中B与C的物质的量相等
(4)该反应的化学平衡常数表达式K=
| c(B)?c(C) |
| c2(A) |
| c(B)?c(C) |
| c2(A) |
0.25
0.25
.(5)T1℃时,保持容器的体积不变,若充入amolA、bmolB、cmolC,达到平衡时C的体积分数为0.4,则a、b、c的取值可以是
bcde
bcde
.a.a=2、b=1、c=2 b.a=0.5、b=1.7、c=1.7
c.a=1、b=1、c=1 d.a=x、b=c=2x(x>0)
e.b=c、a为大于0的任意值.
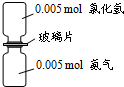 (2012?浦东新区二模)如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
(2012?浦东新区二模)如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )