题目内容
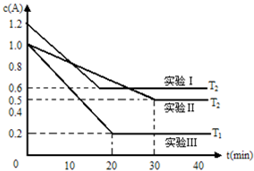 恒容体系,发生如下反应2A(g)?B(g)+xC(?)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图(某课外活动小组一共进行了如图所示的三个实验,其中T1、T2表示不同的反应温度):
恒容体系,发生如下反应2A(g)?B(g)+xC(?)△H,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图(某课外活动小组一共进行了如图所示的三个实验,其中T1、T2表示不同的反应温度):(1)在实验Ⅲ中,0~20min的时间内,v(B)=
(2)根据以上实验事实,完成以下填空:x=
(3)在实验Ⅱ中,当化学反应进行到35min时,下列关于反应体系中的有关说法,正确的是
a.单位时间内生成n mol B的同时生成2n mol A
b.单位时间内生成n mol C的同时消耗2n mol A
c.用A、B、C表示的反应速率的比为2:1:2
d.混合气体中反应物A与生成物B的体积分数之比为2:1
e.混合气体中B与C的物质的量相等
(4)该反应的化学平衡常数表达式K=
| c(B)?c(C) |
| c2(A) |
| c(B)?c(C) |
| c2(A) |
(5)T1℃时,保持容器的体积不变,若充入amolA、bmolB、cmolC,达到平衡时C的体积分数为0.4,则a、b、c的取值可以是
a.a=2、b=1、c=2 b.a=0.5、b=1.7、c=1.7
c.a=1、b=1、c=1 d.a=x、b=c=2x(x>0)
e.b=c、a为大于0的任意值.
| △c |
| △t |
(2)比较实验Ⅰ、Ⅱ,温度相同,A的起始浓度不同,平衡时实验比较实验Ⅰ中A的转化率为50%,实验Ⅱ中A的转化率为50%,A的浓度变化,平衡时A的转化率相同,二者为等效平衡,故反应前后气体的体积不变;由方程式可知,A的化学计量数等于B与C的化学计量数之和,C为气态;
比较实验Ⅱ、Ⅲ,二者A的起始浓度相同、温度不定,温度越高,反应速率越快,最先到达平衡,故温度T1>T2,由图可知温度越高A的转化率越大,温度升高平衡向正反应移动.
(3)由图可知,实验Ⅱ中,当化学反应进行到35min时,可以反应以达平衡状态.
a.单位时间内生成n mol B的同时生成2n mol A,表示正逆反应速率相等,说明反应达平衡状态;
b.单位时间内生成n mol C的同时消耗2n mol A,都表示正反应速率,反应自始至终都按此比较进行;
c.速率之比等于化学计量数之比;
d.由与可知平衡时,A的浓度为0.5mol/L,故A的浓度变化为0.5mol/L,由方程式可知平衡时B的浓度为0.25mol/L;
e.起始时B、C物质的量浓度为0,混合气体中B与C的物质的量之比等于化学计量数之比.
(4)平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;
根据实验实验Ⅱ计算,由图可知,平衡时A的浓度为0.5mol/L,故A的浓度变化为1mol/L-0.5mol/L=0.5mol/L,由方程式可知平衡时B的浓度为0.25mol/L,C的浓度为0.25mol/L,代入平衡常数表达式计算;
(5)由图可知,T1℃时,达平衡时A的浓度为0.2mol/L,A的浓度变化为1mol/L-0.2mol/L=0.8mol/L,由方程式可知原平衡状态C的浓度为
| 1 |
| 2 |
| 0.8mol/L |
| 20min |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:0.02mol/(L.min).
(2)比较实验Ⅰ、Ⅱ,温度相同,A的起始浓度不同,平衡时实验比较实验Ⅰ中A的转化率为
| 0.6mol/L |
| 1.2mol/L |
| 0.5mol/L |
| 1mol/L |
比较实验Ⅱ、Ⅲ,二者A的起始浓度相同、温度不定,温度越高,反应速率越快,最先到达平衡,故温度T1>T2,由图可知温度越高A的转化率越大,温度升高平衡向正反应移动,升高温度平衡向吸热反应移动,故该反应正反应为吸热反应,即△H>0.
故答案为:1,气态,>.
(3)由图可知,实验Ⅱ中,当化学反应进行到35min时,可以反应以达平衡状态.
a.单位时间内生成n mol B的同时生成2n mol A,表示正逆反应速率相等,说明反应达平衡状态,故a正确;
b.单位时间内生成n mol C的同时消耗2n mol A,都表示正反应速率,反应自始至终都按此比较进行,故b正确;
c.速率之比等于化学计量数之比,用A、B、C表示的反应速率的比为2:1:1,故c错误;
d.由与可知平衡时,A的浓度为0.5mol/L,故A的浓度变化为0.5mol/L,由方程式可知平衡时B的浓度为0.25mol/L,故混合气体中反应物A与生成物B的体积分数之比为2:1,故d正确;
e.起始时B、C物质的量浓度为0,混合气体中B与C的物质的量之比等于化学计量数之比为1:1,故d正确.
故选:abde.
(4)平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,所以可逆反应2A(g)?B(g)+C(g)d的平衡常数k=
| c(B)?c(C) |
| c2(A) |
根据实验实验Ⅱ计算,由图可知,平衡时A的浓度为0.5mol/L,故A的浓度变化为1mol/L-0.5mol/L=0.5mol/L,由方程式可知平衡时B的浓度为
| 1 |
| 2 |
| 1 |
| 2 |
| 0.25×0.25 |
| 0.52 |
故答案为:
| c(B)?c(C) |
| c2(A) |
(5)由图可知,T1℃时,达平衡时A的浓度为0.2mol/L,A的浓度变化为1mol/L-0.2mol/L=0.8mol/L,由方程式可知原平衡状态C的浓度为
| 1 |
| 2 |
| 0.4mol/L |
| 1mol/L |
a.若为a=2、b=1、c=2,n(B)≠n(C),故a错误;
b.a=0.5、b=1.7、c=1.7,n(B)═n(C),故b正确;
c.a=1、b=1、c=1,n(B)═n(C),故c正确;
d.a=x、b=c=2x(x>0),n(B)═n(C),故d正确;
e.b=c、a为大于0的任意,n(B)═n(C),故d正确.
故选:bcde.
2、恒温恒容下反应前后体积变化的条件下,改变起始时加入物质的物质的量,只要按化学计量数换算成同一半边对应物质的物质的量与原平衡相同,则达到平衡后与原平衡等效.

(19分)我国《车用燃料甲醇国家标准》的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g) 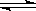 CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。
CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。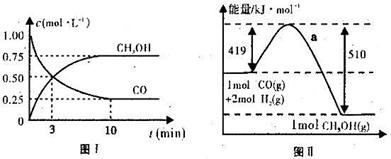
请根据图示回答下列问题:
(1)图I是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=_______________。
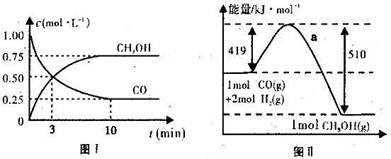
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b。
(3)写出该反应的热化学方程式 。
(4)该反应的平衡常数K的表达式为 ;当温度升高时,该平衡常数K将________(填“增大”、“减小”或“不变”)。
(5)恒容条件下,下列措施中能使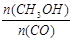 增大的有 。
增大的有 。
A.升高温度 B.充人He气
C.再充入1molCO和2molH2 D.使用催化剂
(6)在恒温条件下,保持CO浓度不变,扩大容器体积,则平衡 (填“逆向移动”、“正向移动”、“不移动”)
(7)在温度、容积相同的三个密闭容器中,按不同方式投料,保持恒温、恒容,测得反应达到平衡时的有关数据如下
| 容器 | 甲 | 乙 | 丙 |
| 投料量 | 1mol CO 、2mol H2 | 1molCH3OH | 2molCH3OH |
| CH3OH的浓度(mol·L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 吸收Q3kJ |
| 体系压强(Pa) | P1 | P2 | P3 |
| 反应物转化率 | α1 | α2 | α3 |
A.c1= c2 B.Q3= 2Q2 C.2 P1<P3
D.α1+α2=1
 E.2α2=α3
E.2α2=α3F.该反应若生成1molCH3OH放出的热量为(Q1+ Q2)kJ
(8)若在一体积可变的密闭容器中充入1mol CO、2mol H2和1molCH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是
(19分)我国《车用燃料甲醇国家标准》的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g) 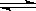 CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。
CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。
请根据图示回答下列问题:
(1)图I是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=_______________。
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b。
(3)写出该反应的热化学方程式 。
(4)该反应的平衡常数K的表达式为 ;当温度升高时,该平衡常数K将________(填“增大”、“减小”或“不变”)。
(5)恒容条件下,下列措施中能使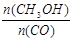 增大的有
。
增大的有
。
A.升高温度 B.充人He气
C.再充入1molCO和2molH2 D.使用催化剂
(6)在恒温条件下,保持CO浓度不变,扩大容器体积,则平衡 (填“逆向移动”、“正向移动”、“不移动”)
(7)在温度、容积相同的三个密闭容器中,按不同方式投料,保持恒温、恒容,测得反应达到平衡时的有关数据如下
|
容器 |
甲 |
乙 |
丙 |
|
投料量 |
1mol CO 、2mol H2 |
1molCH3OH |
2molCH3OH |
|
CH3OH的浓度(mol·L-1) |
c1 |
c2 |
c3 |
|
反应的能量变化 |
放出Q1 kJ |
吸收Q2 kJ |
吸收Q3 kJ |
|
体系压强(Pa) |
P1 |
P2 |
P3 |
|
反应物转化率 |
α1 |
α2 |
α3 |
则下列关系正确的是
A.c1= c2 B.Q3 = 2Q2 C.2 P1<P3
D.α1+α2=1 E.2α2=α3
E.2α2=α3
F.该反应若生成1molCH3OH放出的热量为(Q1+ Q2)kJ
(8)若在一体积可变的密闭容器中充入1mol CO、2mol H2和1molCH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是
 2CO(g) △H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。
2CO(g) △H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。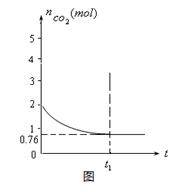
 2CO(g) △H>0
2CO(g) △H>0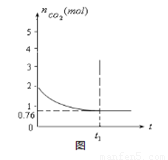
 2CO(g)
△H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。
2CO(g)
△H>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。