网址:http://m.1010jiajiao.com/timu3_id_33084[举报]
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO![]() 、MnO
、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种组成,取该溶液进行如下实验:(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
中的若干种组成,取该溶液进行如下实验:(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(B)在(A)所得溶液中再加入过量碳酸氢铵溶液,有气体生成;同时析出白色沉淀甲;
(C)在(B)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是_______________________________;
(2)一定存在的离子是_______________________________;
(3)判断沉淀乙成分的方法是________________________。
查看习题详情和答案>>某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO![]() 、MnO
、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种组成,取该溶液进行如下实验:
中的若干种组成,取该溶液进行如下实验:
①取适量试液,加入过量盐酸,有气体生成,并得到溶液;
②在①所得溶液中再加入过量碳酸氢铵溶液,有气体生成;同时析出白色沉淀甲;
③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出.
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是________;
(2)一定存在的离子是________;
(3)判断沉淀乙成分的方法是________.
某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO![]() 、MnO
、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
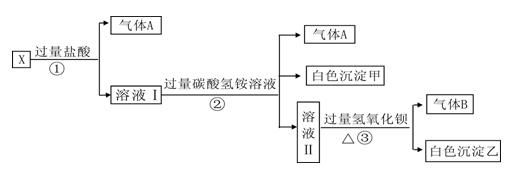
(1)白色沉淀甲是 。
(2)X溶液中一定存在的离子是 。
(3)白色沉淀乙中一定有: ,可能有 证明其是否存在的方法是 。
(4)若将过量的气体A与适量的气体B通入水中,写出反应的离子方程式
查看习题详情和答案>>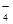 、CO
、CO 、MnO
、MnO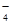 、CO
、CO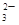 、SO
、SO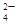 中的若干种离子组成,取溶液进行右图实验:
中的若干种离子组成,取溶液进行右图实验: