摘要:一)常见净化原理:气体的净化可分为物理方法和化学方法.遵循以下原理: ①不损失主体气体,②不引入新杂质,③在密闭容器中进行,④先除易除的气体. 1.物理方法: (1)液化法:利用沸点不同从空气中分离N2和O2. (2)水洗法:利用溶解度不同从N2和NH3中除去NH3,从NO和NO2中除去NO2. △ 2.化学方法: (1)氧化还原法:灼热铜丝网除去混合物中的O2(2Cu+O2=2CuO),CuO除去H2.CO等. (2)酸碱法:NH3和CO2通过碱石灰除去CO2.(CaO+CO2=CaCO3) (3)沉淀法:除去CO2中的H2S通过CuSO4溶液.H2S+CuSO4=CuS↓+H2SO4 (4)最常用的为洗气法: ①用饱和NaCl除去Cl2中的HCl, ②用饱和NaHCO3除去CO2中的HCl.SO2等, ③用酸性高锰酸钾除去气体中的SO2,(如CO2中的SO2) 注意:以下考得比较少: ④用饱和NaHSO3除去SO2中的SO3,[浓硫酸也可除SO3(SO3易溶于浓硫酸)],冷却同样可以除SO3. ⑤用饱和Na2CO3溶液除去乙酸乙酯中的乙醇或乙酸,
网址:http://m.1010jiajiao.com/timu3_id_330152[举报]
SnCl4在催化杂Diels-aider反应、酚甲酰化反直中有重要应用,某化学研究小组欲探究SnCl4的制备.
[参阅资料]
SnCl4在常温下是无色液体,沸点为114℃,遇潮湿空气便发生水解反应,Sn的熔点为231℃.
[实验步骤]
第一步:金属Sn的制备——以锡石SnO2为原料,用过量的焦炭作还原剂,在高温下可制得粗锡.
第二步:SnCl4的制备——用干燥、纯净的C12与熔融的Sn反应制备SnCl4同时放出大量的热.
下图是实验室制备SnCl4的实验装置:

[问题思考]
(1)第一步反应的化学方程式为________.
(2)装置B、C中的药品分别为________.
(3)当反应生成SnCl4时,应熄灭________处的酒精灯,理由是________.
[实验改进]
老师说装置E设计不完整,请你提出修改意见,并说明修改的目的:________.
(2013?江苏)B.[实验化学]
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成.一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取.①分离出甲醇的操作是的
②萃取用到的分液漏斗使用前需
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3 溶液洗涤的目的是
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤.为了防止倒吸,减压过滤完成后应先
查看习题详情和答案>>
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成.一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g?cm-3 | 溶解性 |
| 甲醇 | 64.7 | / | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | / | 0.7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | / | 33~36 | / | 易溶于甲醇、乙醚,微溶于水 |
蒸馏
蒸馏
.②萃取用到的分液漏斗使用前需
检漏
检漏
并洗净,分液时有机层在分液漏斗的上
上
填(“上”或“下”)层.(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3 溶液洗涤的目的是
除去HCl
除去HCl
;用饱和食盐水洗涤的目的是除去少量NaHCO3且减少产物损失
除去少量NaHCO3且减少产物损失
.(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是
dcab
dcab
(填字母).a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤.为了防止倒吸,减压过滤完成后应先
拆去连接抽气泵和吸滤瓶的橡皮管
拆去连接抽气泵和吸滤瓶的橡皮管
,再关闭抽气泵
关闭抽气泵
.化合物A为某矿物样品的主要成分,其质量分数为80%,且A仅由Cu、Fe、S三种元素组成.某研究小组对其组成进行分析,具体实验如下(不考虑杂质的影响):
①准确称取2.3g样品,加入足量的浓硝酸充分溶解后过滤,得到滤液B.
②在B中通入过量的氨气,结果溶液呈深蓝色,同时得到1.07g红褐色沉淀.
③在②的滤液中加入足量盐酸,未见沉淀产生,再滴入足量氯化钡溶液,最后得到4.66g白色沉淀.
已知:Cu2O+2H+=Cu2++Cu+H2O,请回答下列问题:
(1)写出氨气的电子式: ,深蓝色离子的化学式: ,A的化学式: .
(2)工业上常利用该矿物与氧气反应熔炼金属Cu,同时也得到气体C和炉渣(主要成分为Fe2O3).
①在新制的C水溶液中滴加一定量的BaCl2溶液,初始观察不到明显现象,充分振荡后,可观察到有白色沉淀产生,且逐渐增多,请解释其原因 .
②冶炼过程中的最后一步是氧化亚铜与硫化亚铜在高温下作用得到金属铜和气体C,写出该步骤发生反应的化学方程式 .该方法冶炼得到的铜往往含有少量氧化亚铜,请设计实验方案检验铜中是否含有氧化亚铜: .
③炉渣中的氧化铁可用来制备高铁酸钾(K2FeO4).K2FeO4是一种集氧化、吸附、絮凝、杀菌、脱嗅于一体,具有绿色、环保、高效等特点的新型水处理剂.研究发现K2FeO4的氧化性比KMnO4、O3还要强,在中性、酸性溶液中稳定性较差,在碱性溶液中稳定性较好.请写出K2FeO4在强酸性溶液中释放出氧气的离子方程式 .K2FeO4之所以能用于净水,除了能消毒外,另一个原因是 .
查看习题详情和答案>>
①准确称取2.3g样品,加入足量的浓硝酸充分溶解后过滤,得到滤液B.
②在B中通入过量的氨气,结果溶液呈深蓝色,同时得到1.07g红褐色沉淀.
③在②的滤液中加入足量盐酸,未见沉淀产生,再滴入足量氯化钡溶液,最后得到4.66g白色沉淀.
已知:Cu2O+2H+=Cu2++Cu+H2O,请回答下列问题:
(1)写出氨气的电子式:
(2)工业上常利用该矿物与氧气反应熔炼金属Cu,同时也得到气体C和炉渣(主要成分为Fe2O3).
①在新制的C水溶液中滴加一定量的BaCl2溶液,初始观察不到明显现象,充分振荡后,可观察到有白色沉淀产生,且逐渐增多,请解释其原因
②冶炼过程中的最后一步是氧化亚铜与硫化亚铜在高温下作用得到金属铜和气体C,写出该步骤发生反应的化学方程式
③炉渣中的氧化铁可用来制备高铁酸钾(K2FeO4).K2FeO4是一种集氧化、吸附、絮凝、杀菌、脱嗅于一体,具有绿色、环保、高效等特点的新型水处理剂.研究发现K2FeO4的氧化性比KMnO4、O3还要强,在中性、酸性溶液中稳定性较差,在碱性溶液中稳定性较好.请写出K2FeO4在强酸性溶液中释放出氧气的离子方程式
I.A~J分别表示中学化学中常见的一种物质,它们之间相互关系如图1所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素.请填写下列空白:
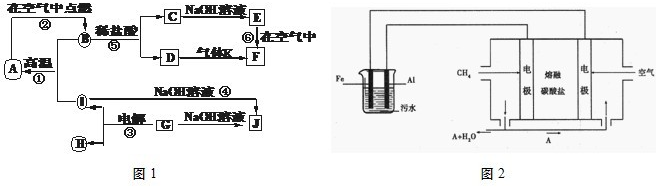
(1)A、B、C、D、E、F六种物质中含有的同一种元素在周期表中位置______,
(2)写出反应④的离子方程式______.
(3)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的pH______7(填“>”、“<”或“=”),用离子方程式表示其原因:______.
II.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图2所示.
(1)电解池阳极的电极反应分别是①______; ②4OH--4e-=2H2O+O2↑.
(2)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.已知负极的电极反应是:CH4+4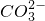 -8e-=5CO2+2H2O
-8e-=5CO2+2H2O
①正极的电极反应是______.
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定.为此电池工作时必须有部分A物质参加循环.则A物质的化学式是______.
(3)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)______ L.
查看习题详情和答案>>
I.A~J分别表示中学化学中常见的一种物质,它们之间相互关系如图1所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素.请填写下列空白:
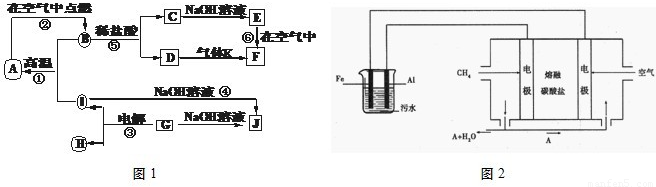
(1)A、B、C、D、E、F六种物质中含有的同一种元素在周期表中位置______,
(2)写出反应④的离子方程式______.
(3)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的pH______7(填“>”、“<”或“=”),用离子方程式表示其原因:______.
II.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图2所示.
(1)电解池阳极的电极反应分别是①______; ②4OH--4e-=2H2O+O2↑.
(2)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.已知负极的电极反应是:CH4+4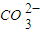 -8e-=5CO2+2H2O
-8e-=5CO2+2H2O
①正极的电极反应是______.
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定.为此电池工作时必须有部分A物质参加循环.则A物质的化学式是______.
(3)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)______ L.
查看习题详情和答案>>

(1)A、B、C、D、E、F六种物质中含有的同一种元素在周期表中位置______,
(2)写出反应④的离子方程式______.
(3)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的pH______7(填“>”、“<”或“=”),用离子方程式表示其原因:______.
II.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图2所示.
(1)电解池阳极的电极反应分别是①______; ②4OH--4e-=2H2O+O2↑.
(2)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极.已知负极的电极反应是:CH4+4
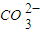 -8e-=5CO2+2H2O
-8e-=5CO2+2H2O①正极的电极反应是______.
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定.为此电池工作时必须有部分A物质参加循环.则A物质的化学式是______.
(3)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)______ L.
查看习题详情和答案>>