摘要:24毫升H2S在30毫升O2中燃烧.在同温同压下.得到的SO2的体积是[D] A.24毫升 B.30毫升 C.20毫升 D.18毫升 [解一]:可采下直接配平法.写出下面的反应方程式: 24H2S+30O2 = 6S+18SO2+24H2O [解二]:采用守恒法: 该题涉及到的两个反应分别是2H2S+3O2 = 2SO2+2H2O和2H2S+O2 = 2S+2H2O.从这两个反应式中可知:H2S中的氢元素全部转移到H2O中.S元素全部转移到SO2和单质S中.而O2中的氧元素全部转移到H2O和SO2中.
网址:http://m.1010jiajiao.com/timu3_id_328537[举报]
 某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚.甲醚是乙醇的同分异构体,其熔点-141.5℃,沸点-24.9℃,在加热条件下可分解成甲烷、乙烷、甲醛等.
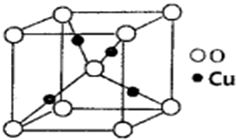
某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚.甲醚是乙醇的同分异构体,其熔点-141.5℃,沸点-24.9℃,在加热条件下可分解成甲烷、乙烷、甲醛等.(1)如图是Cu的某种氧化物的晶胞结构示意图,氧的配位数为
4
4
.(2)乙醇的沸点比甲醚高,其主要原因是
乙醇形成分子间氢键
乙醇形成分子间氢键
.(3)甲醛分子中碳原子轨道的杂化类型为
sp2
sp2
.(4)储氢材料化合物A是乙烷的等电子体,其相对分子质量为30.8,且A是由第二周期两种氢化物形成的化台物.加热A会缓慢释放氢气,同时A转化为化合物B,B是乙烯的等电子体.化合物A的结构式为


5NA
5NA
.