摘要:21.化学平衡移动原理.同样也适用于其他平衡.已知在氨水中存在下列平衡. NH3+H2O NH3·H2O NH4++OH- (1)向氨水中加入MgCl2固体时.平衡向 移动.OH-的浓度 . NH4+的浓度 . (2)向氨水中加入浓盐酸.平衡向 移动.此时溶液中浓度减小的粒子有 . . . (3)向浓氨水中加入少量NaOH固体.平衡向 移动.此时发生的现象 . 22. 由氢气和氧气反应生成1mol水蒸气放热241.8kJ.写出该反应的热化学方程式 . 若1g水蒸气转化成液态水时放热2.444KJ.则反应H2(g) + 1/2O2(g) == H2O(l)的 △H= kJ·.
网址:http://m.1010jiajiao.com/timu3_id_326405[举报]
化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:
NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH
NH![]() +OH-
+OH-
(1)向氨水中加入MgCl2固体时,平衡向_______移动,OH-的浓度_______,NH![]() 的浓度_______。
的浓度_______。
(2)向氨水中加入浓盐酸,平衡向_______移动,此时溶液中浓度减小的粒子有_______、_______、_______。
(3)向浓氨水中加入少量NaOH固体,平衡向_______移动,此时发生的现象是_______。
查看习题详情和答案>>(6分)化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:NH3+H2O NH3·H2O
NH
![]() +OH-
+OH-
(1)向氨水中加入MgCl2固体时,平衡向______移动,OH-的浓度_____,NH4+的浓度_______。
(2)向氨水中加入浓盐酸,平衡向______移动;
(3)向浓氨水中加入少量NaOH固体,平衡向_____移动,此时发生的现象是__________。
查看习题详情和答案>>
(6分)化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:NH3+H2O 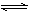 NH3·H2O
NH3·H2O 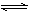 NH
NH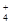 +OH-
+OH-
(1)向氨水中加入MgCl2固体时,平衡向______移动,OH-的浓度_____,NH4+的浓度_______。
(2)向氨水中加入浓盐酸,平衡向______移动;
(3)向浓氨水中加入少量NaOH固体,平衡向_____移动,此时发生的现象是__________。
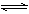 NH3·H2O
NH3·H2O 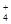 +OH-
+OH- 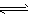 NH3·H2O
NH3·H2O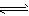 NH4++OH-
NH4++OH-