网址:http://m.1010jiajiao.com/timu3_id_322343[举报]
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
(2)实验①和②的目的是
(3)写出实验③的化学反应方程式
| ||
| ||
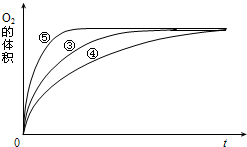
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.分析上图能够得出的实验结论是
 (2011?顺德区模拟)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(2011?顺德区模拟)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为
(3)实验①和②的目的是
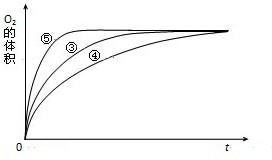
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
分析上图能够得出的实验结论是
汽车为推动人类文明、生活方便舒适起着重要作用,但同时也恶化了自然生态环境。汽车每年排放的一氧化碳、碳氢化合物、一氧化氮等有害气体占大气污染总量的60%以上。
(1)一氧化氮与一氧化碳都是汽车尾气中的有害气体,它们在催化转换器中能反应氮气和二氧化碳,对此反应,下列说法中正确的是( )
A.使用催化剂不能加大反应速率 B.升高温度能加大反应速率
C.改变压强对反应速率没有影响 D.降低压强能加大反应速率
(2)假设辛烷气对空气的体积之比(在相同条件下)为a,要使辛烷完全燃烧,amax是 。
(3)①若辛烷气对空气的体积之比大于amax,2mol辛烷燃烧生成的有害气体的含量为xmol时,其反应的化学方程式为 。
②当辛烷气对空气体积之比小于amax时,则尾气所污染大气的有害气体增多的是 ,产生此气体的化为方程式为 。
II、食盐中含有碘酸钾。
已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32―=2I-+S4O62-。
(1)若检验食盐中所含碘酸钾,可利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳检验生成的碘时,用到的主要玻璃仪器有 。
(2)测定加碘食盐中碘的含量:
a.称取a g食盐并加蒸馏水使其完全溶解;
b.将所得溶液用稀硫酸酸化,再加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,用1.0×10-3mol/L Na2S2O3溶液进行滴定,当消耗20.0mLNa2S2O3溶液时达到滴定终点。则加碘食盐样品中的碘元素含量是 mg/kg(以含a的代数式表示)。
(3)若向食盐溶液中加入淀粉溶液和KI溶液,振荡。溶液无变化。然后再滴入1滴稀H2SO4,振荡,溶液变蓝色
①用离子方程式表示实验中产生蓝色现象的可能原因 。
②根据此实验结果,请对(2)的实验结果作出简要评价: 。(填“偏大”或“偏小”)
查看习题详情和答案>>(1)甲同学利用如图1所示装置(在A、B间增加一盛有浓硫酸的洗气瓶)制备NO2并验证其性质.装置①用于实验室制备NH3,用装置②制备过量O2.A装置中相应药品在催化加热时发生反应的化学方程式是
| ||
| △ |
| ||
| △ |
(2)乙同学利用图2所示装置合成SO3,B处冰水冷却的U型管中的固体出现.C中若盛放K2Cr2O7溶液,则在C中发生的氧化还原反应的离子方程式是
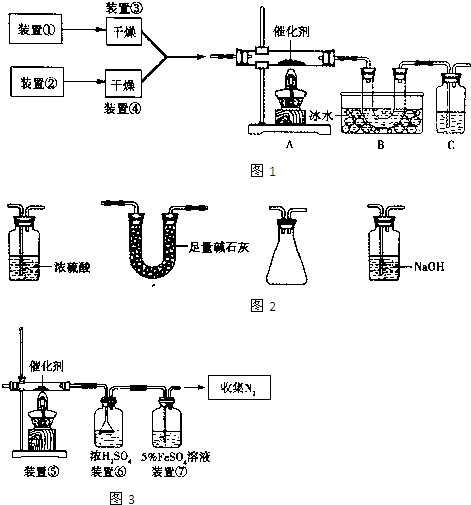
(3)丙同学采用图3所示装置拟验证NO能被氨气还原并测算其转化率(装置①、装置②分别制NO和NH3),将上述装置A、B、C分别换成下列⑤、⑥、⑦.
请回答:装置⑦的作用可能是
| 2016×6 |
| 2688×5 |
| 2016×6 |
| 2688×5 |
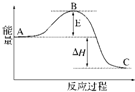 2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:(1)图中A、C分别表示
(2)图中△H=
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式
(4)已知单质硫的燃烧热为296kJ?mol-1,计算由S(s)生成3mol SO3(g)的△H (要求计算过程).
SO2(g)+
| 1 |
| 2 |
3s(s)+
| 9 |
| 2 |
SO2(g)+
| 1 |
| 2 |
3s(s)+
| 9 |
| 2 |