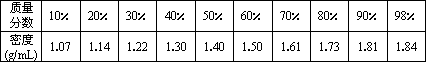摘要:溶液中溶质质量分数的计算 溶质的质量分数是溶质质量与溶液质量之比.初中化学中常用百分数来表示.溶液中溶质质量分数的计算式如下: 溶质的质量分数=×100% 溶质质量分数的计算题可以有: (1)已知溶质和溶剂的质量.求溶液的质量分数. (2)已知溶液的质量和它的质量分数.求溶液里所含溶质和溶剂的质量. (3)将一已知浓度的溶液加入一定量的水进行稀释.或加入固体溶质.求稀释后或加入固体后的溶液的质量分数.
网址:http://m.1010jiajiao.com/timu3_id_3213[举报]
质量分数不同的硫酸溶液其密度不相同,对照表如下:
将10mL98%浓硫酸中加水稀释至100mL,取10mL该稀硫酸与足量锌反应制取氢气,请按要求完成系列问题的解答(计算结果保留一位小数):
(1)10mL98%的浓硫酸中含 g H2SO4.
(2)列式计算消耗金属锌的质量.
(3)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是 .10mL水和10mL质量分数为b%的硫酸溶液混合,混合后溶液的质量分数应该在 至 之间.
查看习题详情和答案>>
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
(1)10mL98%的浓硫酸中含
(2)列式计算消耗金属锌的质量.
(3)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是
质量分数不同的硫酸溶液其密度不相同,对照表如下:
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
将10mL98%浓硫酸中加水稀释至100ml,取10mL该稀硫酸与足量锌反应制取氢气,请按要求完成系列问题的解答(计算结果保留一位小数):
(1)10mL98%的浓硫酸中含 -----gH2SO4。
(2)列式计算消耗金属锌的质量。
查看习题详情和答案>>质量分数不同的硫酸溶液其密度不相同,对照表如下:
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
将10mL98%浓硫酸中加水稀释至100ml,取10mL该稀硫酸与足量锌反应制取氢气,请按要求完成系列问题的解答(计算结果保留一位小数):
(1)10mL98%的浓硫酸中含 gH2SO4。
(2)列式计算消耗金属锌的质量。
查看习题详情和答案>>