摘要:(1)已知1 gC2H2气体完全燃烧生成CO2气体和液态水.放出50.0kJ的热量.试写出表示其燃烧热的热化学方程式: . (2)水的电离平衡曲线图如图所示:①若以A点表示25℃时水的电离平衡时的离子浓度,当温度上升至100℃时.水的电离平衡状 态到B点.则此时水的离子积从 增加 到 . ②将pH=8的Ba(OH)2溶液与pH=5的 稀盐酸混合.并保持在100℃的恒温.若使混 合液的pH=7.则盐酸和Ba(OH)2溶液的体积 比为 .
网址:http://m.1010jiajiao.com/timu3_id_320410[举报]
 (2011?大兴区二模)短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.
(2011?大兴区二模)短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.(1)写出元素F在周期表中的位置
第3周期第IVA族
第3周期第IVA族
.(2)由元素ABC组成的18电子物质,是假酒中常见的有毒物质之一,其电子式为


(3)已知这样两反应 G(s)+C2(g)=GC2(g)△H1=-296KJ?mol-1,2GC3(g)?2GC2(g)+C2(g)△H2=+198KJ?mol-1 2G(s)+3C2(g)?2GC3(g)△H3=
-790KJ?mol-1
-790KJ?mol-1
(4)对于可逆反应:2GC2(g)+C2(g)?2GC3(g)△H=aKJ?mol-1 图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.GC3%T1时平衡常数K1、T2时平衡常数K2,则K1
>
>
K2(>、<、=).T2时在2L密闭容器中充入4moLGC2和3moLC2,在一定条件下达到平衡时GC2的转化率为90%,则这时的平衡常数数值是135
135
.(5)D2FC3溶液与E2(GC4)3溶液混合产生两种均溶于DCA溶液的难溶物质,写出两溶液混合所发生的离子反应方程式
3SiO32-+2Al3++6H2O=2Al(OH)3↓+3H2SiO3↓
3SiO32-+2Al3++6H2O=2Al(OH)3↓+3H2SiO3↓
(6)向Ba(AGC3)2溶液中滴加足量A2C2产生23.3克白色沉淀时,反应中电子转移总数物质的量为
0.2mol
0.2mol
.
短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.
(1)写出元素F在周期表中的位置 .
(2)由元素ABC组成的18电子物质,是假酒中常见的有毒物质之一,其电子式为 .
(3)已知这样两反应 G(s)+C2(g)=GC2(g)△H1=-296KJ?mol-1,2GC3(g)?2GC2(g)+C2(g)△H2=+198KJ?mol-1 2G(s)+3C2(g)?2GC3(g)△H3=
(4)对于可逆反应:2GC2(g)+C2(g)?2GC3(g)△H=aKJ?mol-1 图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.GC3%T1时平衡常数K1、T2时平衡常数K2,则K1 K2(>、<、=).T2时在2L密闭容器中充入4moLGC2和3moLC2,在一定条件下达到平衡时GC2的转化率为90%,则这时的平衡常数数值是 .
(5)D2FC3溶液与E2(GC4)3溶液混合产生两种均溶于DCA溶液的难溶物质,写出两溶液混合所发生的离子反应方程式
(6)向Ba(AGC3)2溶液中滴加足量A2C2产生23.3克白色沉淀时,反应中电子转移总数物质的量为 .
 查看习题详情和答案>>
查看习题详情和答案>>
(1)写出元素F在周期表中的位置 .
(2)由元素ABC组成的18电子物质,是假酒中常见的有毒物质之一,其电子式为 .
(3)已知这样两反应 G(s)+C2(g)=GC2(g)△H1=-296KJ?mol-1,2GC3(g)?2GC2(g)+C2(g)△H2=+198KJ?mol-1 2G(s)+3C2(g)?2GC3(g)△H3=
(4)对于可逆反应:2GC2(g)+C2(g)?2GC3(g)△H=aKJ?mol-1 图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.GC3%T1时平衡常数K1、T2时平衡常数K2,则K1 K2(>、<、=).T2时在2L密闭容器中充入4moLGC2和3moLC2,在一定条件下达到平衡时GC2的转化率为90%,则这时的平衡常数数值是 .
(5)D2FC3溶液与E2(GC4)3溶液混合产生两种均溶于DCA溶液的难溶物质,写出两溶液混合所发生的离子反应方程式
(6)向Ba(AGC3)2溶液中滴加足量A2C2产生23.3克白色沉淀时,反应中电子转移总数物质的量为 .
 查看习题详情和答案>>
查看习题详情和答案>>
短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.
(1)、写出元素F在周期表中的位置________.
(2)、由元素ABC组成的18电子物质,是假酒中常见的有毒物质之一,其电子式为________.
(3)、已知这样两反应G(s)+C2(g) GC2(g) ΔH1=-296 KJ·mol-1,2GC3(g)
GC2(g) ΔH1=-296 KJ·mol-1,2GC3(g)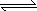 2GC2(g)+C2(g) ΔH2=+198 KJ·mol-1
2GC2(g)+C2(g) ΔH2=+198 KJ·mol-1
则2G(s)+3C2(g)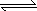 2GC3(g) ΔH3=________.
2GC3(g) ΔH3=________.
(4)、对于可逆反应:2GC2(g)+C2(g)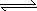 2GC3(g) ΔH=a KJ·mol-1图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.
2GC3(g) ΔH=a KJ·mol-1图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.
GC3%
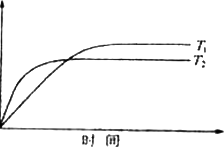
T1时平衡常数K1、T2时平衡常数K2,则K1________K2(>、<、=).
T2时在2 L密闭容器中充入4 moL GC2和3 moL C2,在一定条件下达到平衡时GC2的转化率为90%,则这时的平衡常数数值是________.
(5)、D2FC3溶液与E2(GC4)3溶液混合产生两种匀溶于DCA溶液的难溶物质,写出两溶液混合所发生的离子反应方程式________.
(6)向Ba(AGC3)2溶液中滴加足量A2C2产生23.3克白色沉淀时,反应中电子转移总数物质的量为________.