摘要:13.缠有某种金属丝的铁钉插在含有酚酞的食盐水中.可看到在贴近金属丝一边的溶液中出现红色.则金属丝可能是 ( ) A.Mg B.Al C.Zn D.Cu
网址:http://m.1010jiajiao.com/timu3_id_320080[举报]
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
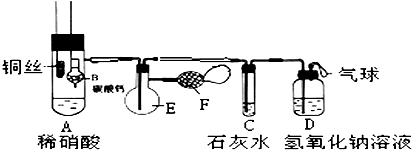
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先排出去其中的空气.你第一步实验操作为:
确定E中空气已被赶尽的实验现象为:
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为
(3)如何证明E中收集的是NO而不是H2?
(4)装置D的作用
查看习题详情和答案>>

(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先排出去其中的空气.你第一步实验操作为:
B装置中CaCO3放入硝酸中
B装置中CaCO3放入硝酸中
;确定E中空气已被赶尽的实验现象为:
C中石灰水变浑浊
C中石灰水变浑浊
.(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
;(3)如何证明E中收集的是NO而不是H2?
将F气球中空气压入E中,有红棕色气体生成
将F气球中空气压入E中,有红棕色气体生成
;一段时间后,C中白色沉淀溶解,其原因是2HNO3+CaCO3═Ca(NO3)2+2H2O
2HNO3+CaCO3═Ca(NO3)2+2H2O
;(4)装置D的作用
吸收多余的NO、NO2
吸收多余的NO、NO2
.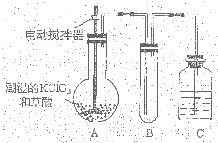 二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用下图所示装置模拟工业制取及收集ClO2.(夹持仪器已省略).回答问题:
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用下图所示装置模拟工业制取及收集ClO2.(夹持仪器已省略).回答问题:(1)B必须添加温度控制装置,应补充的装置是
(2)C中试剂为
(3)A中反应产物有某种盐、ClO2和CO2等,写出相关化学方程式
ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行下列实验:准确量取ClO2溶液10mL,稀释成100mL试样;量取V1 mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,反应原理:2Na2S2O3+I2→Na2S4O6+2NaI,消耗Na2S2O3溶液V2mL.
(4)滴定过程中至少须进行两次平行测定的原因是
(5)到达滴定终点时指示剂的颜色变化为
(6)原ClO2溶液的浓度为
(2013?长春模拟)将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如下图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)
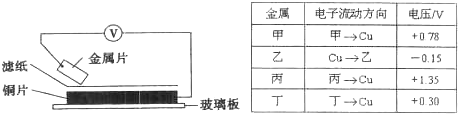
依据记录数据判断,下列结论中正确的是( )

依据记录数据判断,下列结论中正确的是( )
查看习题详情和答案>>
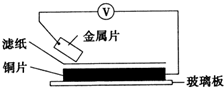 将洁净的金属片A、B、C、D分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下: 将洁净的金属片A、B、C、D分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下:
|
查看习题详情和答案>>
二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料.
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:

(1)Fe2O3与H2SO4反应的离子方程式是
(2)甲溶液中除含TiO2+之外还含有的金属阳离子有
(3)加Fe的作用是
方法2:TiCl4水解生成TiO2?xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛.
(4)①TiCl4水解生成TiO2?xH2O的化学方程式为
②检验TiO2?xH2O中Cl-是否被除净的方法是
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:TiO2
TiCl4
Ti
反应②的方程式是
查看习题详情和答案>>
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:

(1)Fe2O3与H2SO4反应的离子方程式是
Fe2O3+6H+=2Fe3++3H2O
Fe2O3+6H+=2Fe3++3H2O
.(2)甲溶液中除含TiO2+之外还含有的金属阳离子有
Fe3+、Fe2+
Fe3+、Fe2+
.(3)加Fe的作用是
将Fe3+转化为Fe2+
将Fe3+转化为Fe2+
.方法2:TiCl4水解生成TiO2?xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛.
(4)①TiCl4水解生成TiO2?xH2O的化学方程式为
TiCl4+(x+2)H2O?TiO2?xH2O↓+4HCl
TiCl4+(x+2)H2O?TiO2?xH2O↓+4HCl
;②检验TiO2?xH2O中Cl-是否被除净的方法是
取少量水洗液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净
取少量水洗液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净
.Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:TiO2
| ① |
| ② |
| Mg800℃ |
反应②的方程式是
TiCl4+2Mg
2MgCl2+Ti
| ||
TiCl4+2Mg
2MgCl2+Ti
,该反应需要在Ar气氛中进行,请解释原因:
| ||
防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用
防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用
.