题目内容
(2013?长春模拟)将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如下图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)
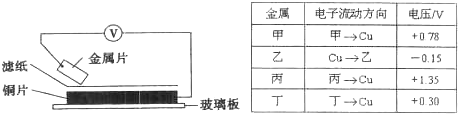
依据记录数据判断,下列结论中正确的是( )

依据记录数据判断,下列结论中正确的是( )
分析:根据原电池中电子的流向判断金属的强弱,电压值越大,金属的活泼性越强,以此解答各题.
解答:解:甲-Cu连接时,电子从甲→Cu,所以甲的金属性大于铜;
乙-Cu连接时,电子从Cu→乙,所以乙的金属性小于铜;
丙-Cu连接时,电子从丙→Cu,所以丙的金属性大于铜;
丁-Cu连接时,电子从丁→Cu,所以丁的金属性大于铜;
A、金属乙的金属性小于铜,所以金属乙不能从硫酸铜溶液中置换出铜,故A错误;
B、甲的金属性大于铜,乙的金属性小于铜,所以金属性是甲大于乙,甲、乙形成合金时,将该合金露置在空气中,甲先被腐蚀,故B正确;
C、甲、丙、丁的金属性均强于Cu,但是电压越大,金属性越强,所以活泼性是:丙>甲>丁,只有乙的活泼性弱于铜,所以在四种金属中乙的还原性最弱,故C错误;
D、活泼性是:丙>甲>丁,甲、丁若形成原电池时,活泼金属甲作负极,故D错误.
故选B.
乙-Cu连接时,电子从Cu→乙,所以乙的金属性小于铜;
丙-Cu连接时,电子从丙→Cu,所以丙的金属性大于铜;
丁-Cu连接时,电子从丁→Cu,所以丁的金属性大于铜;
A、金属乙的金属性小于铜,所以金属乙不能从硫酸铜溶液中置换出铜,故A错误;
B、甲的金属性大于铜,乙的金属性小于铜,所以金属性是甲大于乙,甲、乙形成合金时,将该合金露置在空气中,甲先被腐蚀,故B正确;
C、甲、丙、丁的金属性均强于Cu,但是电压越大,金属性越强,所以活泼性是:丙>甲>丁,只有乙的活泼性弱于铜,所以在四种金属中乙的还原性最弱,故C错误;
D、活泼性是:丙>甲>丁,甲、丁若形成原电池时,活泼金属甲作负极,故D错误.
故选B.
点评:本题考查常见金属的活动性顺序的比较方法以及金属的电化学腐蚀及防护,题目难度中等,注意把握原电池的工作原理,注意加强对数据分析能力的培养.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
